Page 137 - 《中国药科大学学报》2026年第2期
P. 137
第 57 卷第 2 期 张 靖,等:齐多夫定通过促进脂肪酸氧化改善高脂饮食诱导的大鼠代谢紊乱 263
肪酸氧化增强、肝脏脂肪变性减轻及血脂水平改 组及 AZT 给药组血清乳酸水平未观察到显著升
善,提示 AZT 的代谢改善作用可能部分通过调控 高,表明 AZT 干预未引起乳酸蓄积。在线粒体功
PPAR 信号通路实现。 能方面,与对照组相比,HFD 模型组与 AZT 给药组
3.7 AZT 在改善代谢的同时未诱发线粒体毒性 的肝脏 ATP 水平呈现上升趋势,各组间线粒体膜电
为评估此治疗剂量下 AZT 是否产生线粒体毒 位保持稳定,无显著差异。以上结果表明,本研究
性,检测了终点空腹血清乳酸水平与肝脏线粒体功 采用的干预方案下,AZT 在改善代谢的同时,未损
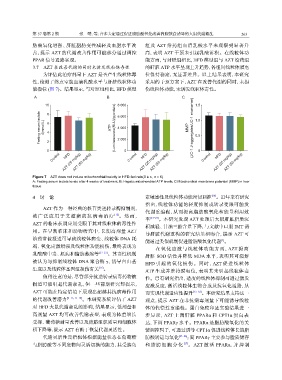
能指标 (图 7)。结果显示,与对照组相比,HFD 模型 伤线粒体功能,未诱发线粒体毒性。
A B C
10 8 8 000 1.5
Fasting serum lactate /(mmol/L) 6 4 ATP (Luminescence(RLU)/g protein) 4 000 MMP (JC-1 J-aggregates/JC-1 monomer) 1.0
6 000
0.5
2 000
0 2 0 0
AZT (50 mg/kg)
HFD
AZT (50 mg/kg)
HFD
Control AZT (25 mg/kg) Control AZT (25 mg/kg) Control AZT (25 mg/kg)
HFD
AZT (50 mg/kg)
Figure 7 AZT does not induce mitochondrial toxicity in HFD-fed rats( x ± s, n = 6)
A: Fasting serum lactate levels after 4 weeks of treatment; B: Hepatic mitochondrial ATP levels; C:Mitochondrial membrane potential (MMP) in liver
tissue
4 讨 论 素敏感性及线粒体功能密切调控 。近年来有研究
[20]
指出,线粒体功能的轻度抑制或转录受限可触发
AZT 作为一种经典的核苷类逆转录酶抑制剂,
代谢重编程,从而提高脂肪酸氧化和能量利用效
被 广 泛 应 用 于 艾 滋 病 的 抗 病 毒 治 疗 [12] 。 然 而 ,
率 [21−23] 。本研究发现 AZT 处理后大鼠肝脏脂质沉
AZT 的临床长期应用受限于其对线粒体的毒性作
积减轻、甘油三酯含量下降,与文献中口服 IMT 诱
用。在早期临床和动物研究中,长期高剂量 AZT
导肝脏代谢重构的研究结果相吻合,提示 AZT 可
给药常被报道可导致线粒体病变、线粒体 DNA 耗
能通过类似机制促进脂肪酸氧化代谢 。
[7]
竭、氧化应激增强及线粒体功能损伤,最终表现为
在氧化应激与线粒体功能方面,AZT 提高
乳酸酸中毒、肌病和脂肪萎缩等 [13−15] 。其毒性机制 肝脏 SOD 活性并降低 MDA 水平,表明其可缓解
被认为与抑制线粒体 DNA 聚合酶 γ、诱导自由基
HFD 引起的氧化损伤。同时,AZT 促进线粒体
生成以及线粒体基因组损伤有关 。
[16]
ATP 生成并维持膜电位,表明其未引起线粒体毒
值得注意的是,尽管部分抗逆转录病毒药物被 性。已有研究指出,适度的线粒体抑制可通过激发
报道可能引起代谢紊乱,但一些前期研究却提示, 应激反应,激活线粒体生物合成及抗氧化通路,从
AZT 可能在特定情境下展现出超越其抗病毒作用 而实现代谢适应性提升 [23−24] 。本研究结果支持这一
的代谢改善潜力 [9−11, 17−19] 。本研究系统评估了 AZT 观点,提示 AZT 在非抗病毒剂量下可能诱导线粒
对 HFD 大鼠代谢紊乱的影响,结果显示,低剂量和 体的代偿性重编程。蛋白免疫印迹实验结果进一
高剂量 AZT 均可改善代谢表型,表现为体重增长 步显示,AZT 上调肝脏 PPARα 和 CPT1α 蛋白表
受抑、葡萄糖耐量改善以及脂肪组织质量和细胞体 达,下调 PPARγ 水平。PPARα 是脂肪酸氧化的关
积下降等,提示 AZT 有助于恢复代谢灵活性。 键调控因子,可通过诱导 CPT1α 促进线粒体长链脂
代谢灵活性是指机体根据能量状态在葡萄糖 肪酸转运与氧化 [25−26] ;而 PPARγ 主要参与脂质储存
与脂肪酸等不同底物间灵活切换的能力,其受胰岛 和 脂 肪 细 胞 分 化 [27] 。 AZT 激 活 PPARα, 并 抑 制