Page 117 - 《中国药科大学学报》2026年第2期
P. 117
第 57 卷第 2 期 孙嘉荣,等:小分子化合物 Lyb24 与二氢乳清酸脱氢酶 PyrD 的相互作用研究 243
Insight Evaluation 软件以 1∶1 Langmuir 模型进行动 白。通过 SDS-PAGE 分析,目标蛋白在 500 mmol/L
力学拟合,获得结合动力学与亲和力参数。 IM 洗脱液中仅呈现一条主带;进一步通过 Image
2.3 DCIP 比色法检测 PyrD 活性 J 灰度扫描,蛋白主峰占总面积 94.96%。
2.3.1 标准曲线的建立 DCIP 的标准曲线在反应 M 1 2 3 4 5
缓冲液(100 mmol/L Tris、0.1 mmol/L EDTA-Na 、 180 kD
130 kD
2
200 µmol/L CoQ0,pH 8.0)中建立。在 96 孔板中将 100 kD
DCIP 母液梯度稀释为 18.75~600 µmol/L 系列浓 70 kD
55 kD
度,每孔反应体积为 100 µL,使用酶标仪读取 600
40 kD
nm 处 吸 收 度 ( A 600 ) 。 以 DCIP 浓 度 为 横 坐 标 , 35 kD
A 60 0 为纵坐标进行线性回归分析,所得标准曲线方
25 kD
程用于后续酶活性反应速率计算。
2.3.2 酶促反应体系与动力学测定 总反应体积 15 kD
为 100 µL,于 96 孔板中进行。反应混合液包含:
10 kD
100 mmol/L Tris、0.1 mmol/L EDTA-Na 、200 µmol/L
2
CoQ0、150 µmol/L DCIP 及 0.3 µmol/L 重组 PyrD Figure 1 SDS-PAGE electrophoresis of purified PyrD protein
蛋白。抑制剂组预先加入 Lyb24 至终浓度 0、17.5、 Lane M: Protein marker; Lane 1: 10 mmol/L imidazole eluate; Lane 2:
20 mmol/L imidazole eluate; Lane 3: 50 mmol/L imidazole eluate;
35 及 70 µmol/L,37 ℃ 预孵育 30 min。反应由加入 Lane 4: 100 mmol/L imidazole eluate; Lane 5: 500 mmol/L imidazole
eluate
底物 DHO 启动,其终浓度分别为 50、100、200 及
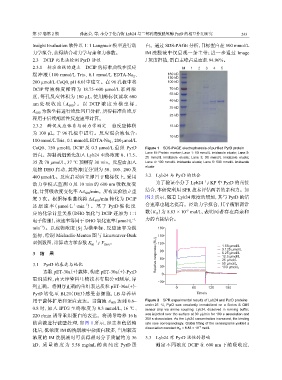
400 µmol/L。反应启动后立即置于酶标仪上,采用 3.2 Lyb24 与 PyrD 的结合
动力学模式监测 0 及 10 min 的 600 nm 吸收度变 为了验证小分子 Lyb24 与 KP 中 PyrD 的直接
化,计算吸收度变化率 ΔA 600 /min。所有实验独立重 结合,本研究利用 SPR 技术评估两者的亲和力。如
复 3 次。根据标准曲线将 ΔA 600 /min 转化为 DCIP 图 2 所示,随着 Lyb24 浓度的增加,其与 PyrD 的结
−1
−1
还 原 速 率 ( µmol·L ·min ) 。 基 于 PyrD 催 化 反 合速率也随之提高。经动力学拟合,其平衡解离常
−5
应的化学计量关系(DHO 氧化与 DCIP 还原为 1∶1 数(K )为 8.83 × 10 mol/L,表明两者存在高亲和
D
−1
电子传递),该速率等同于 DHO 氧化速率(µmol·L · 力的直接结合。
min )。以底物浓度 [S] 为横坐标、反应速率为纵 180
−1
坐标,绘制 Michaelis-Menten 图与 Lineweaver-Burk 150
双倒数图,计算动力学参数 K 与 V max 。 120 1.56 μmol/L
m
6.25 μmol/L
3 结 果 Relative response (RU) 90 3.125 μmol/L
12.5 μmol/L
60
50 μmol/L
3.1 PyrD 的表达与纯化 30 25 μmol/L
100 μmol/L
选取 pET-30a(+)载体,构建 pET-30a(+)-PyrD
0
重组质粒,由天津擎科生物技术有限公司测序,序
−30
列正确。将测序正确的重组表达质粒 pET-30a(+)- 0 60 120 180
PyrD 转化至 BL21(DE3)感受态细胞,LB 培养基 Time/s
用于菌体扩增和蛋白表达。当菌液 A 60 0 达到 0.6~ Figure 2 SPR experimental results of Lyb24 and PyrD proteins
under 25 ℃, PyrD was covalently immobilized on a Series S CM5
0.8 时,加入 IPTG 至终浓度为 0.3 mmol/L,16 ℃、 sensor chip via amine coupling. Lyb24, dissolved in running buffer,
220 r/min 诱导重组蛋白的表达。将诱导培养 16 h was injected over the surface at 30 µL/min for 100 s association and
200 s dissociation. As the Lyb24 concentration increased, the binding
的菌液进行破壁处理,如图 1 所示,经亲和色谱纯 rate rose correspondingly. Global fitting of the sensorgrams yielded a
−5
化后,低浓度 IM 的洗脱液中杂蛋白较多,当用较高 dissociation constant K D = 8.83 × 10 mol/L
浓度的 IM 洗脱液时可获得相对分子质量约为 36 3.3 Lyb24 对 PyrD 活性的影响
kD、 质 量 浓 度 为 5.58 mg/mL 的 高 纯 度 PyrD 蛋 测定不同浓度 DCIP 在 600 nm 下的吸收度,