Page 43 - 《中国药科大学学报》2026年第1期
P. 43
第 57 卷第 1 期 邴天德,等:乳酸脱氢酶 A 抑制剂的设计、合成与生物活性 37
中间体 27 为原料,通过重氮化碘代反应得中间体 的溴苄 34 为原料,与三甲基硅叠氮发生取代反应
31。经过 Sonogashira 偶联反应生成三甲基硅炔取 制得中间体 35。随后将中间体 35 和中间体 33 通
代的噻唑甲酸乙酯中间体 32。在 TBAF 中脱去三 过“点击化学”反应制得中间体 36。最后经水解反
甲基硅基,制得中间体 33。以对位不同取代基取代 应,得到目标化合物 17~25。
O O S
Br i
O O N
O NH 2
26 27
iii
O NO 2
NH 2 ii N N
R R H H
28a−28i 29a−29i
O S O O S O
O N N N iv HO N N N
H
H
R H H
R
30a−30i 8−16
28a−30a, 8: R=H; 28d−30d, 11: R=Br; 28g−30g, 14: R=OCF 3 ;
28b−30b, 9: R=F; 28e−30e, 12: R=OCH 3 ; 28h−30h,15: R=CONH 2 ;
28c−30c, 10: R=Cl; 28f−30f, 13: R=CF 3 ; 28i−30i, 16: R=SO 2 NH 2 ;
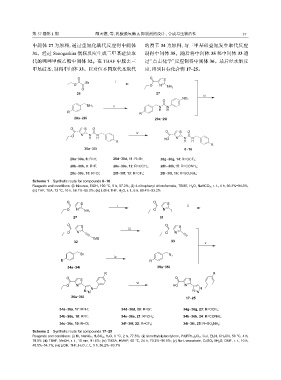
Scheme 1 Synthetic route for compounds 8−16
Reagents and conditions: (i) thiourea, EtOH, 100 °C, 5 h, 57.2%; (ii) 4-nitrophenyl chloroformate, TBME, H 2 O, NaHCO 3 , r. t., 4 h, 66.3%−94.3%;
(iii) THF, TEA, 72 °C, 10 h, 58.1%−65.3%; (iv) LiOH, THF, H 2 O, r. t., 6 h, 89.4%−93.2%
O S i O S
O N NH 2 O N I ii
27 31
O S O S
iii
O N O N
TMS
32 33 v
Br
iv N 3
R R
34a−34i 35a−35i
R R
O S O S
O N vi HO N
N N N N N N
36a−36i 17−25
34a−36a, 17: R=H; 34d−36d, 20: R=Br; 34g−36g, 23: R=OCF 3 ;
34b−36b, 18: R=F; 34e−36e, 21: R=CH 3 ; 34h−36h, 24: R=CONH 2 ;
34c−36c, 19: R=Cl; 34f−36f, 22: R=CF 3 ; 34i−36i, 25: R=SO 2 NH 2 ;
Scheme 2 Synthetic route for compounds 17−25
Reagents and conditions: (i) KI, NaNO 2 , H 2 SO 4 , H 2 O, 0 °C, 2 h, 77.5%; (ii) trimethylsilylacetylene, Pd(PPh 3 ) 2 Cl 2 , CuI, Et 3 N, CH 3 CN, 50 °C, 4 h,
78.9% (iii) TBAF, MeOH, r. t., 10 min, 91.5%; (iv) TMSA, HMAP, 60 °C, 24 h, 73.2%−96.0%; (v) Na-L-ascorbate, CuSO 4 ·5H 2 O, DMF, r. t., 10 h,
40.5%−54.1%; (vi) LiOH, THF, H 2 O, r. t., 5 h, 56.2%−93.7%