Page 36 - 《中国药科大学学报》2025年第5期
P. 36
568 学报 Journal of China Pharmaceutical University 2025, 56(5): 566 − 571 第 56 卷
本,将样本依次置于 5%NaNO 溶液、10%Al(NO ) mL,混合均匀后,于 60 ℃ 水浴反应 15 min。反应
2
3 3
溶液各浸泡 10 min,擦干表面试液,置于载玻片上, 结束后,立即置于冰水浴中 2 min 终止反应,随后加
滴加 10%NaOH 溶液显色,于显微镜下观察并拍照。 入冰乙酸 5 mL。采用紫外-可见分光光度计,于
2.2.3 水合氯醛透化结合亚硝酸钠-硝酸铝-氢氧化 532 nm 波长处测定溶液的吸收度。
钠法染色 水合氯醛作为一种良好的透明剂,能够 2.3.4 总黄酮含量检测 量取 “2.3.2”项提取浓缩
溶解细胞内的淀粉粒、蛋白质、脂肪等物质,增加细 液 2 mL,以芦丁为标准品进行总黄酮含量检测。
胞膜和细胞壁的通透性 ,常用于中药材粉末鉴 将所取提取浓缩液置于 60 ℃ 水浴中挥干,加入
[10]
定。为此引入水合氯醛透化步骤,以新鲜黄芪根为 60% 乙 醇 2 mL 使 其 完 全 溶 解 , 随 后 转 移 至
材料,采用徒手切片法制备横切面样本,将其置于 10 mL 量瓶内,加 5%NaNO 溶液 0.3 mL,振荡均
2
载玻片上,滴加水合氯醛试液,于酒精灯上加热,保 匀,室温下静置 6 min;再吸取 10%Al(NO ) 溶液
3
3
持微沸 10 s,重复滴加试液和加热操作,直至切片呈 0.3 mL, 振 荡 均 匀 后 继 续 静 置 6 min; 接 着 加 入
透明状,置于显微镜下观察并拍照。最后,将透化 4%NaOH 溶液 4 mL,振荡均匀,室温下静置 15 min;
后的切片,按“2.2.2”项染色流程操作,置于显微镜 最后用 60% 乙醇定容至 10 mL 刻度线,摇匀。采
下观察并拍照。 用紫外-可见分光光度计,于 510 nm 波长处测定溶
2.3 黄芪不同部位含量检测 液的吸收度。
2.3.1 组织分离 取新鲜黄芪,用刀纵向切口,将 2.3.5 统计学分析 每组均平行测定 3 次,检测值
中心木质部和韧皮部分离,剥离木质部,再将周皮 以 x± s表示。采用 Excel 软件对数据进行双尾 t
和韧皮部分离,分别剪成小段,50 ℃ 烘干至恒重后 检验,P<0. 05 表示有统计学意义上的显著差异,
粉碎,过 65 目筛。检测黄芪各部位的过筛部分和 P <0.001 为非常显著差异。利用 GraphPad5. 01 软
筛余部分总皂苷、总黄酮以及黄芪甲苷含量。 件进行图表绘制。
2.3.2 黄芪甲苷含量检测 参考 2020 年版《中华
3 结 果
人民共和国药典》 制备供试液和标准品溶液,采
[5]
用 高 效 液 相 色 谱 法 进 行 检 测 ( high-performance 3.1 皂苷显微组织化学定位
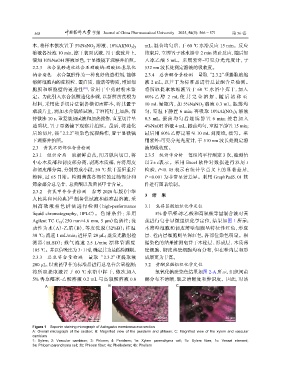
liquid chromatography, HPLC) 。 色 谱 条 件 : 采 用 5% 香草醛-冰乙酸和高氯酸等量混合液对黄
Agilent TC C (250 mm×4.6 mm,5 μm)色谱柱;流 芪进行皂苷显微组织化学定位,结果如图 1 所示:
18
动性为水(A)-乙腈(B),等度洗脱(32%B);柱温 木薄壁细胞和韧皮薄壁细胞呈特征性红色,形成
30 ℃;流速 1 mL/min;进样量 20 μL;蒸发光散射检 层、栓内层细胞则呈深红色,各部位染色明显。根
测器(ELSD);载气流速 2.5 L/min;漂移管温度 据染色的结果推测皂苷于木栓层、形成层、木质薄
105 ℃。并以信噪比为 3∶1 时,确定其为最低检测限。 壁细胞、韧皮薄壁细胞均有分布,但在栓内层和形
2.3.3 总皂苷含量检测 量取 “2.3.2”项提取液 成层更为丰富。
200 μL,以黄芪甲苷为标准品进行总皂苷含量检测; 3.2 黄酮显微组织化学定位
将所取提取液置于 60 ℃ 水浴中挥干,依次加入 氢氧化钠法染色结果如图 2-A 所示,组织间黄
5% 香草醛冰-乙酸溶液 0.2 mL 与高氯酸溶液 0.8 酮分布不清晰,缺乏清晰度和辨识度。因此,对该
A B C
1 4b 3b 1a 1c
2 3a
1b
3
4a
4 100 μm 40 μm 40 μm
Figure 1 Saponin staining micrograph of Astragalus membranaceus section
A: Overall micrograph of the section; B: Magnified view of the periderm and phloem; C: Magnified view of the xylem and vascular
cambium
1: Xylem; 2: Vascular cambium; 3: Phloem; 4: Periderm; 1a: Xylem parenchyma cell; 1b: Xylem fiber; 1c: Vessel element;
3a: Phloem parenchyma cell; 3b: Phloem fiber; 4a: Phelloderm; 4b: Phellem