Page 116 - 《中国药科大学学报》2025年第5期
P. 116
648 学报 Journal of China Pharmaceutical University 2025, 56(5): 645 − 653 第 56 卷
[23]
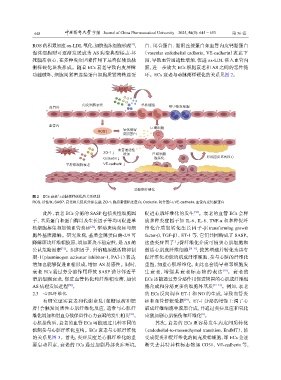
ROS 的积累加速 ox-LDL 氧化,加快泡沫细胞形成 , 白、闭合蛋白、黏附连接蛋白如血管内皮钙黏蛋白
泡沫细胞则可逐渐发展成为 AS 病变典型标志-坏 (vascular endothelial cadherin, VE-cadherin)表达下
死脂质核心,在多种炎症因素作用下最终促使动脉 调,导致血管通透性增加,促进 ox-LDL 渗入血管内
粥样硬化斑块形成。随着 ECs 衰老导致内皮屏障 膜,进一步放大 ECs 细胞衰老和 AS 之间的恶性循
功能破坏,细胞间紧密连接蛋白如胞质紧密粘连蛋 环。ECs 衰老与动脉粥样硬化的关系见图 2。
SASP
内皮细胞衰老 单核细胞
血管外 嗜中性粒细胞
血管内 巨噬细胞
ROS↑ 氧化低密
度脂蛋白
SASP ZO-1 ↓ 血管通透性 巨噬细胞
增加
Occludin ↓ 泡沫化 形成脂质坏死核心
平滑肌细胞衰老 VE-cadherin ↓
动脉粥样硬化
图 2 ECs 衰老与动脉粥样硬化的关系机制
ROS:活性氧;SASP:衰老相关促炎分泌表型;ZO-1:胞质紧密粘连蛋白;Occludin:闭合蛋白;VE-cadherin:血管内皮钙黏蛋白
[30]
此外,衰老 ECs 分泌的 SASP 包括炎性细胞因 促进心肌纤维化的发生 。衰老的血管 ECs 会释
子、基质蛋白和蛋白酶以及生长因子等均可促进单 放多种炎症因子如 IL-6、IL-8、TNF-α 和多种促纤
核细胞募集和加快血管炎症 ,驱动斑块炎症与细 维化介质如转化生长因子-β(transforming growth
[26]
胞外基质降解。研究发现,基质金属蛋白酶-2/9 可 factor-β,TGF-β)、ET-1 等,它们共同构成了 SASP。
降解斑块纤维帽胶原,增加斑块不稳定性,是 AS 的 这些炎症因子与促纤维化介质可损害心肌细胞和
公认危险因素 。组织因子、纤溶酶原激活物抑制 激活心肌成纤维细胞 [30−31] ,使其增殖并转化为具有
[27]
剂-1(plasminogen activator inhibitor-1,PAI-1)表达 促纤维化功能的肌成纤维细胞,参与心脏的纤维化
增加也能够促进血栓形成,增加 AS 易感性。同时, 重塑,加重心肌纤维化,由此也会诱导相邻细胞发
衰老 ECs 通过旁分泌作用释放 SASP 诱导邻近平 生衰老,增强其衰老标志物的表达 [10] 。衰老的
滑肌细胞衰老,促进血管钙化和纤维帽变薄,加快 ECs 还能通过旁分泌作用促进周围的心肌成纤维细
[28]
AS 病理发展进程 。 胞合成和分泌更多的细胞外基质 [32−33] 。例如,衰老
2.3 心肌纤维化 的 ECs 反向调节 ET-1 和 NO 的生成,导致血管炎
有研究证实衰老和代谢紊乱(如糖尿病和肥 症和血管舒张受损 。ET-1 分泌的增加上调了心
[34]
胖)会触发间质性心肌纤维化反应,通常与心肌纤 脏成纤维细胞中胶原合成,并通过炎症反应和氧化
[29]
[6]
维化增加和射血分数保留性心力衰竭的发生相关 。 应激加剧心肌损伤和纤维化 。
心肌损伤后,衰老的血管 ECs 可能通过几种不同的 其次,衰老的 ECs 更容易发生内皮间质转化
机制参与心脏纤维化重构。ECs 衰老与心肌纤维化 (endothelial-to-mesenchymal transition,EndMT),转
的关系见图 3。首先,炎症反应是心肌纤维化的重 变成促炎和促纤维化的间充质样细胞,即 ECs 会逐
要启动因素,衰老的 ECs 通过加剧局部炎症环境, 渐失去其特异性标志物如 CD31、VE-cadherin 等,