Page 11 - 《中国药科大学学报》2025年第4期
P. 11
第 56 卷第 4 期 贾佳庆,等:核酸模式识别机制及其化学干预的研究进展 407
HO
N N O
N O H 2 N N N O N
N N H 2 N N H
N
NH 2
Resiquimod Imiquimod Telratolimod
TLR7/8激动剂 TLR7激动剂 TLR7/8激动剂
H 2 N
N
N
NH 2 O
H 2 N N N N N N O OH O N H
N
N N F N N O O P O O N NH O
F HO Cl HO S O O
F F HO O O
Enpatoran ZYS-1 O Inarigivir soproxil CBL0137
TLR7/8抑制剂 ADAR1抑制剂 O RIG-I激动剂 ZBP1激动剂
O NH 4
O P S Cl
N
O N N H N N F O H N OH O
N
N N N HO S OH
O F N N H N O O
S P O
O
NH 4
E-7766 Hydroxychloroquine sulfate
STING激动剂 TLR9抑制剂
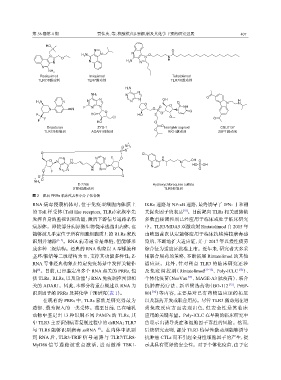
图 2 靶向 PRRs 临床代表性小分子化合物
RNA 病毒侵袭机体时,位于免疫型细胞内体膜上 IKKε 通路与 NF-κB 通路,最终诱导了 IFN- Ⅰ和相
的 Toll 样受体(Toll like receptors, TLRs)家族率先 关促炎因子的表达 。目前靶向 TLRs 相关通路的
[10]
发挥自身的监视识别功能,激活下游信号通路杀伤 多数直接调控剂已经应用于临床或处于临床研究
病原体。即使部分病原微生物侥幸逃逸出内体,也 中。TLR3/MDA5 双激动剂 Rintatolimod 自 2015 年
能够被几乎定位于所有细胞细胞质上的 RLRs 家族 由欧盟首次认定能够应用于临床抗埃博拉病毒感
识别并清除 [6−7] 。RNA 病毒通常是单链,但能够形 染后,不断地扩大适应证,并于 2017 年以慢性疲劳
成多种二级结构。经典的 RNA 构象以 A 型螺旋和 综合征为适应证批准上市。近年来,研究者大多采
茎环/假结等二级结构为主,支撑其功能多样性;Z- 用联合用药的策略,不断拓展 Rintatolimod 的其他
RNA 等非经典构象在特定免疫场景中发挥关键作 适应证。此外,针对靶点 TLR3 的临床研究还涉
用 。目前,已经鉴定出多个 RNA 相关的 PRRs,包 及免疫调控剂(Rintatolimod [11−12] 、Poly-ICLC [13] )、
[8]
括 TLRs、RLRs,以及功能与 RNA 免疫调控密切相 个体化疫苗(NeoVax [14] 、MAGE-A3 肽疫苗)、联合
关的 ADAR1。因此,本部分将重点概述以 RNA 为 抗肿瘤药疗法、新型候选药物(BO-112 [15] 、PrEP-
识别因子的 PRRs 及其化学干预研究(表 1)。 001 )等内容,主要是对已有药物适应证的拓展
[16]
在现有的 PRRs 中,TLRs 家族是研究得最为 以及新药开发或联合用药。尽管 TLR3 激动剂在增
透彻、最为深入的一类受体。截至目前,已在哺乳 强免疫反应方面表现出色,但安全性是其临床
动物中鉴定出 13 种识别不同 PAMPs 的 TLRs,其 应用的关键考量。Poly-ICLC 在早期的临床研究中
中 TLR3 主要识别病毒复制过程中的 dsRNA;TLR7 曾显示出诱导炎症和细胞因子毒性的风险。然而,
与 TLR8 能够识别病毒 ssRNA 。在内体中识别 后续研究表明,部分 TLR3 特异性激动剂能够诱导
[9]
到 RNA 后,TLR3-TRIF 信号通路与 TLR7/TLR8- 抗肿瘤 CTLs 而不引起全身性细胞因子的产生,提
MyD88 信号通路被重点激活,进而激活 TBK1- 示其具有更好的安全性。对于个体化疫苗,由于它