Page 191 - 《水产学报》2026年第3期
P. 191
3 期 吴海霞,等:草鱼 GCRV-II 抗原检测胶体金试剂盒研发与应用 50 卷
层析方向
tomographic direction 抗原
antigen
胶体金标记 VP35#8
样品垫 结合垫 检测线 质控线 吸水垫 gold labeled VP35#8
sample pad conjugate test line control line absorbent pad
VP35#8
羊抗鼠 IgG
(a) gold anti-mouse IgG
样品孔 检测线 质控线
sample hole test line control line
层析方向
sample flow
(b)
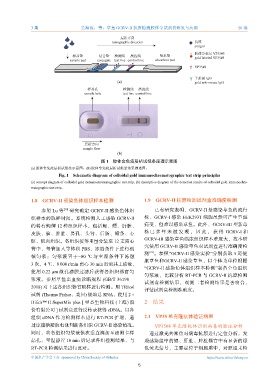
图 1 胶体金免疫层析试纸条原理示意图
(a) 胶体金免疫层析试纸条示意图,(b) 胶体金免疫层析试纸条结果描述图。
Fig. 1 Schematic diagram of colloidal gold immunochromatographic test strip principles
(a) concept diagram of colloidal gold immunochromatographic test strip, (b) descriptive diagram of the detection results of colloidal gold immunochro-
matographic test strip.
1.8 GCRV-II 感染鱼体组织样本检测 1.9 GCRV-II 抗原检测试剂盒准确度检测
参照 Lu 等 [10] 研究确定 GCRV-II 感染鱼体组 已有研究表明,GCRV-II 是感染草鱼的流行
织样本的取样时间。系统检测人工感染 GCRV-II 株,GCRV-I 感染 HEK293T 细胞虽然可产生空斑
的稀有鮈鲫 12 种组织样本,包括鳃、鳔、肝脏、 病变,但难以感染草鱼。此外,GCRV-III 型新毒
皮肤、脑、脾脏、鼻孔、头肾、后肠、鳍条、心 株 已 多 年 未 被 发 现 , 因 此 , 获 得 GCRV-I 和
脏、肌肉组织。各组织按等重量分装至 12 支离心 GCRV-III 感染草鱼临床组织样本难度大,故本研
究使用 GCRV-II 感染草鱼对试剂盒进行准确度检
管中,每管加入等体积 PBS,冰浴条件下进行机
测 [31] 。参照“GCRV-II 感染实验”分别获取 5 尾健
械匀浆;匀浆液置于−80 ℃ 与室温条件下冻融
康草鱼和GCRV-II 感染草鱼,以个体为单位根据
3 次,4 ℃、8 000 r/min 离心 30 min 后取其上清液,
“GCRV-II 感染鱼体组织样本检测”制备全鱼组织
使用 0.22 μm 微孔滤膜过滤后获得各组织器官匀
匀浆液,比较分析 RT-PCR 与 GCRV-II 抗原检测
浆液。参照草鱼出血病诊断规程 (GB/T 36190—
试剂盒检测结果,观测二者检测结果是否吻合,
2018) 对上述各组织器官取样进行检测。用 TRIzol
评估试剂盒检测准确度。
试剂 (Thermo Fisher,美国) 提取总 RNA,使用 2 ×
Hifair™ II SuperMix plus [ 翌圣生物科技 (上海) 股 2 结果
份有限公司 ] 试剂盒进行反转录获得 cDNA。以各
组织 cDNA 作为检测样本进行 RT-PCR 扩增,通 2.1 VP35 单克隆抗体验证结果
过琼脂糖凝胶电泳判断各组织 GCRV-II 感染情况。 VP35#8 单克隆抗体识别病毒的验证分析
同时,将各组织匀浆液依次垂直滴加至速测卡样 通过激光共聚焦对病毒抗原进行定位分析,发
品孔,室温静置 10 min 后记录各组检测结果,与 现感染组中的鳃、肝脏、脾脏器官中有显著的绿
RT-PCR 检测结果进行比对。 色荧光信号,主要定位于细胞质中,对照组未检
中国水产学会主办 sponsored by China Society of Fisheries https://www.china-fishery.cn
5