Page 104 - 《水产学报》2026年第3期
P. 104
3 期 水 产 学 报 50 卷
Control Heat 子-细胞因子受体相互作用、糖酵解/糖异生及肌动
蛋白细胞骨架调控。
3 讨论
50 μm 1 50 μm 2 水产养殖业正面临全球变暖的巨大威胁,了
Control Heat 解 CHS 对鱼类能量代谢的调节机制将有助于制定
应对策略。能量是鱼类维持细胞乃至组织正常生
理功能的物质基础,保持能量稳态对鱼类在极端
环境下维持自身健康及存活尤为重要 。鱼类能
[30]
5 μm 3 5 μm 4 量代谢易受水温影响,水温过高或过低均可使其
能量代谢紊乱并造成组织损伤 [31-32] 。糖脂代谢是鱼
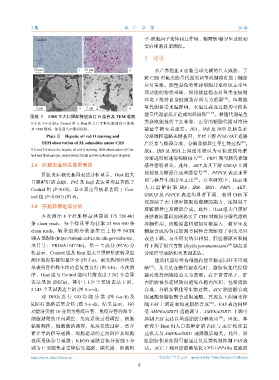
图版 Ⅱ CHS 下大口黑鲈肝脏油红 O 染色及 TEM 观察
类获取能量的主要来源,正常的糖脂代谢对维持
1~2 及 3~4 分别示 Control 组与 Heat 组大口黑鲈肝脏油红 O 染色
及 TEM 观察;黑色箭头示脂质沉积。 能量平衡至关重要。IRA、IRB 及 IRS1 是胰岛素
Plate Ⅱ Hepatic oil red O staining and 分泌调控通路关键基因,并经下游 PI3K/AKT 通路
[33]
TEM observation of M. salmoides under CHS 广泛参与糖原合成、分解及糖异生等生物过程 。
1-2 and 3-4 show the hepatic oil red O staining TEM observation of Con- 及 上调通常被认为可促进胰岛素
IRA、IRB IRS1
trol and Heat groups, respectively; black arrows indicate lipid droplets. [26]
分泌进而加速葡萄糖摄入 ,PBP1 则与胰岛素敏
2.4 肝脏炎症相关基因表达 感性密切相关。此外,AKT 及其下游 GSK3β 上调
[34]
肝脏炎症相关基因表达分析显示,Heat 组大 则被视为糖原合成增强信号 ,PEPCK 表达水平
[35]
口黑鲈肝脏 IκBβ、P65 及 Iκκβ 表达量均显著低于 则与糖异生强度呈正比 。在本研究中,Heat 组
Control 组 (P<0.05),IL-8 表达量极显著低于 Con- 大 口 黑 鲈 肝 脏 IRA、 IRB、 IRS1、 PBP1、 AKT、
trol 组 (P<0.001) (图 4)。 GSK3β 及 PEPCK 表达均显著下调,表明 CHS 不
仅抑制了大口黑鲈摄取葡萄糖的能力,还抑制了
2.5 肝脏转录组学分析
肝脏糖异生及糖原合成。此外,Heat 组大口黑鲈
本次测序 8 个肝脏样品共获取 175 728 401 肝脏糖原蓄积加剧揭示了 CHS 对糖原分解代谢的
条 clean reads,每个样品平均获取 21 966 050 条 抑制作用,而糖原蓄积增加对糖摄入、糖异生及
clean reads。转录组测序数据集已上传至 NCBI 糖原合成的负反馈调节同样合理解释了相关基因
SRA 数据库 (https://submit.ncbi.nlm.nih.gov/subs/sra, 表达下调。与本研究结果相似,肝脏糖原蓄积同
项目号:PRJNA1347746)。第一主成分 (PCA) 分 样下调了拟穴青蟹 (Scylla paramamosain) [36] 胰岛素
析显示,Control 组及 Heat 组大口黑鲈肝脏转录组 分泌信号通路相关基因表达。
测序数据集被明显区分 (图 5-a),聚类热图分析结 脂质代谢对维持细胞内能量稳态同样不可或
果表明各组样本组内重复性良好 (图 5-b)。本次测 缺 。尤其是在糖代谢紊乱时,脂肪氧化代偿供
[37]
序,Heat 组与 Control 组间共筛选出 3 262 个差异 能对维持细胞稳态尤为重要。在正常情况下,肝
表达基因 (DEGs),其中 1 119 个基因表达下调, 内脂肪被快速周转而避免在胞内沉积,包括脂肪
2 143 个基因表达上调 (图 5-c~d)。 合成、分解及氧化等生物过程。ACC 脂肪酸合成
对 DEGs 进 行 GO 功 能 分 类 (图 6-a~b) 及 限速酶是脂肪酸合成限速酶,其表达上调通常伴
[38]
KEGG 通路富集分析 (图 6-c~d)。结果显示,GO 随 FAS 上调进而加速脂肪合成 。FAS 表达同样
功能分类前 10 分别为免疫应答、免疫应答的调节、 受 AMPKα/SIRT1 通路调节,AMPKα/SIRT1 上调可
细胞黏附的正向调控、免疫系统过程调控、细胞 抑制 FAS 表达以增强脂肪分解效应 。因此,本
[39]
黏附调控、细胞激活调控、免疫系统过程、整合 研究中 Heat 组大口黑鲈肝脏 FAS 与 ACC 相反表
素介导的信号通路、细胞运动的正向调控及细胞 达模式与 AMPKα/SIRT1 通路激活相关。此外,肝
表面受体信号通路;KEGG 通路富集分析前 5 分 脏脂肪积累加剧可能通过负反馈机制抑制 FAS 表
别为 C 型凝集素受体信号通路、碳代谢、细胞因 达。ACC 上调对脂肪酸氧化 CPT-1/PPARα 通路的
https://www.china-fishery.cn 中国水产学会主办 sponsored by China Society of Fisheries
6