Page 108 - 《水产学报》2026年第3期
P. 108
3 期 水 产 学 报 50 卷
Heatmap
PCA 0.827 0.964 0.488 0.877 0.928 0.934 0.929 1.000 N-4 1.00
200 C 0.815 0.964 0.522 0.872 0.958 0.967 1.000 0.929 N-3 0.90
T 0.80
0.803 0.967 0.500 0.849 0.979 1.000 0.967 0.934 N-2 0.70
PC2(16.25%) 0 0.754 0.950 0.502 0.831 1.000 0.979 0.958 0.928 N-1 0.60
0.50
0.930 0.879 0.621 1.000 0.831 0.849 0.872 0.877 H-4
−200 0.617 0.528 1.000 0.621 0.502 0.500 0.522 0.488 H-3
0.848 1.000 0.528 0.879 0.950 0.967 0.964 0.964 H-2
−200 0 200 400
PC1(54.89%) 1.000 0.848 0.617 0.930 0.754 0.803 0.815 0.827 H-1
(a) H-1 H-2 H-3 H-4 N-1 N-2 N-3 N-4
(b)
3 262 type
3 000 all 40
down
up 30
DGE 基因计数 DGE gene counts 2 000 1 119 −lg(FDR) 20 significant
2 143
up
normal
down
1 000
0 10 0
NC0 vs. HT1
−5 0 5
比较组别
compare group log 2 (FC)
(c) (d)
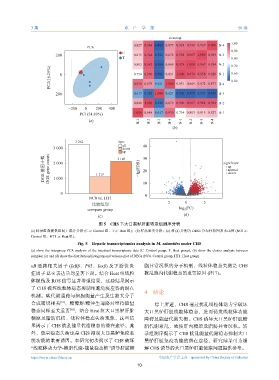
图 5 CHS 下大口黑鲈肝脏转录组测序分析
(a) 转录组数据集组间主成分分析 (C 示 Control 组,T 示 Heat 组);(b) 样品聚类分析;(c) 和 (d) 分别为 DEGs 分布柱状图及火山图 (NC0 示
Control 组,HT1 示 Heat 组)。
Fig. 5 Hepatic transcriptomics analysis in M. salmoides under CHS
(a) show the intergroup PCA analysis of the intestinal transcriptome data (C. Control group, T. Heat group); (b) show the cluster analysis between
samples; (c) and (d) show the distribution histogram and volcano plot of DEGs (NC0. Control group, HT1. Heat group).
κB 通路相关因子 (IκBβ、P65、Iκκβ) 及下游促炎 脂异常沉积的分子机制,线粒体稳态失衡是 CHS
症因子 IL-8 表达量均显著下调。结合 Heat 组线粒 扰乱胞内代谢稳态的重要原因 (图 7)。
体损伤及 ROS 信号显著增强结果,这些结果揭示
了 CHS 破坏线粒体稳态抑制细胞免疫应答的潜在
4 结论
机制。碳代谢通路与细胞能量产生及生物大分子
[61]
合成密切相关 ,糖酵解/糖异生通路对维持能量 综上所述,CHS 通过扰乱线粒体动力学破坏
[62]
稳态同样至关重要 ,结合 Heat 组大口黑鲈肝脏 大口黑鲈肝脏线粒体稳态,进而诱发线粒体功能
糖原及脂肪沉积、线粒体稳态失衡现象,这些结 障碍及能量代谢失衡。CHS 诱导大口黑鲈肝脏糖
果揭示了 CHS 扰乱能量代谢稳态的潜在途径。此 脂代谢紊乱,致使肝内糖原及脂肪异常沉积。转
外,能量稳态失衡也是 CHS 抑制大口黑鲈免疫系 录组测序揭示了 CHS 扰乱能量代谢稳态抑制大口
统功能的重要诱因。本研究初步揭示了 CHS 破坏 黑鲈肝脏免疫功能的潜在途径,研究结果可为缓
“线粒体动力学-糖脂代谢-能量稳态轴”诱导肝脏糖 解 CHS 诱导的大口黑鲈肝脏健康问题提供参考。
https://www.china-fishery.cn 中国水产学会主办 sponsored by China Society of Fisheries
10