Page 107 - 《水产学报》2026年第3期
P. 107
3 期 王笑然,等:慢性热应激诱导大口黑鲈肝脏线粒体功能障碍及糖脂异常沉积 50 卷
1.5 盾表达可能与 SIRT1 无法有效激活 PGC-1α 转录
Control Heat
有关;其核心机制可能为:高浓度 ROS 通过抑制
*
*
*
的去乙酰化过
***
HATs 活性干扰了
对
SIRT1
PGC-1α
相对表达量 relative expression level 1.0 程,导致能量感知系统与线粒体生物合成通路间
的 解 偶 联 , 最 终 抑 制 了 线 粒 体 的 生 物 合 成 。
作为线粒体分裂的核心动力蛋白,与招募
DRP1
0.5
因子
分别介导线粒体内、外膜融合,二者协同
MFN1 FIS1 协同介导线粒体分裂过程 [53] ;OPA1 与
执行线粒体融合过程 [27] ;P62 可经泛素结合域识
0
IκBβ P65 Iκκβ TNF-α IL-8 IL-1β 别受损线粒体,与 LC3 共同形成自噬体完成受损
[54]
基因 线粒体清除 。上述基因共同构成了线粒体稳态
genes
调节网络。在本研究中,Heat 组大口黑鲈肝脏
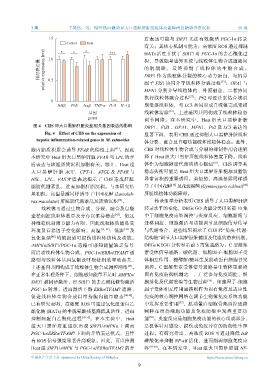
图 4 CHS 对大口黑鲈肝脏炎症相关基因表达的影响 及 表达均
DRP1、FIS1、OPA1、MFN1、P62 LC3
Fig. 4 Effect of CHS on the expression of 显著下调,表明 CHS 通过抑制大口黑鲈肝脏线粒
hepatic inflammation-related genes in M. salmoides
体分裂、融合及自噬功能破坏线粒体稳态。此外,
胞内脂质积累会诱导 FFAR 代偿性上调 [41] 。因此 CHS 对线粒体生物合成与分裂的抑制作用合理解
本研究中 Heat 组大口黑鲈肝脏 FFAR 与 LPL 的矛 释了 Heat 组大口黑鲈肝脏线粒体密度下降。线粒
[55]
盾表达与该组脂质沉积加剧有关。综上,Heat 组 体作为细胞糖脂代谢的核心枢纽 ,CHS 诱导其
大 口 黑 鲈 肝 脏 ACC、 CPT-1、 ATGL 及 FFAR 与 稳态失衡可能是 Heat 组大口黑鲈肝脏糖原及脂肪
HSL、LPL、FAS 矛盾表达揭示了 CHS 造成肝脏 异常蓄积的重要诱因。类似的,高温暴露同样诱
脂肪代谢紊乱,进而加剧肝脂沉积。与本研究结 导了中国花鲈 [14] 及花斑裸鲤 (Gymnocypris eckloni) [44]
果相似,高温暴露同样诱导了中国花鲈 (Lateolab- 肝脏线粒体功能障碍。
rax maculatus) 肝脏脂代谢紊乱及脂质沉积 。 转录组学分析表明 CHS 诱导了大口黑鲈肝脏
[14]
线粒体可通过生物合成、分裂、融合及自噬 转录水平的变化,DEGs GO 功能分类排名前 10 集
[43]
途径调控线粒体数量及分布以维持稳态 ,但这 中于细胞免疫应答调控与炎症反应、细胞黏附与
种维稳机制调节能力有限,因此线粒体功能易受 迁移调控、细胞激活与功能调节及细胞信号传导
环境及营养因子变化影响,高温 [14, 44] 、低渗 [45] 及 与代谢整合,这些结果揭示了 CHS 经“免疫-代谢-
氧化鱼油 [46] 均被报道可损伤线粒体结构及功能。 结构轴”调节大口黑鲈肝脏健康及代谢的潜在机制。
AMPKα/SIRT1/PGC-1α 通路可感知能量缺乏信号 DEGs KEGG 分析显示前 5 富集通路为:C 型凝集
而启动线粒体生物合成,PGC-1α/ERRα/TFAM7 通 素受体信号通路、碳代谢、细胞因子-细胞因子受
路则与线粒体基因复制及呼吸链组装驱动相关, 体相互作用、糖酵解/糖异生及肌动蛋白细胞骨架
上述基因共同构成了线粒体生物合成调控网络 。 调控。C 型凝集素受体信号通路是生物体重要的
[47]
在正常生理条件下,细胞感知能量不足时 AMPKα/ 固有免疫防御机制之一,广泛参与免疫调控、细
[56]
SIRT1 被同步激活,经 SIRT1 的去乙酰化修饰激活 胞活化及代谢重编等生物过程 ,细胞因子-细胞
PGC-1α 转录,进而激活下游 ERRα/TFAM7 通路、 因子受体相互作用通路则作为固有免疫及适应性
促进线粒体生物合成以维持胞内能量稳态 [48-49] 。 免疫的核心调控网络在调节生物体免疫系统功能
[57]
已有研究表明,高浓度 ROS 可通过氧化组蛋白乙 中发挥重要作用 ,肌动蛋白细胞骨架调控通路
酰化酶 (HATs) 的半胱氨酸残基降低其活性,进而 同样在维持细胞功能及免疫防御中发挥重要功
[58]
抑制组蛋白乙酰化过程 [50-52] 。在本实验中,Heat 能 。炎症反应是细胞免疫功能的核心组成部分,
组大口黑鲈肝脏组织出现 SIRT1/AMPKα 上调而 是机体针对感染、损伤或免疫异常的防御性生理
PGC-1α/ERRα/TFAM7 下调的矛盾表达模式,且伴 过程。有研究指出,高浓度 ROS 可通过降低 IκB
有 ROS 信号强度显著升高现象。因此,可以推测 磷酸化来抑制 NF-κB 活化,进而削弱细胞免疫应
Heat 组 SIRT1/AMPK 与 PGC-1α/ERRα/TFAM7 的矛 答 [59-60] 。在本研究中,Heat 组大口黑鲈肝脏 NF-
中国水产学会主办 sponsored by China Society of Fisheries https://www.china-fishery.cn
9