Page 93 - 《中国药科大学学报》2026年第2期
P. 93
第 57 卷第 2 期 李佳慧,等:载厚朴酚达妥西单抗及三苯基膦双重修饰免疫脂质体对神经母细胞瘤的靶向治疗作用 219
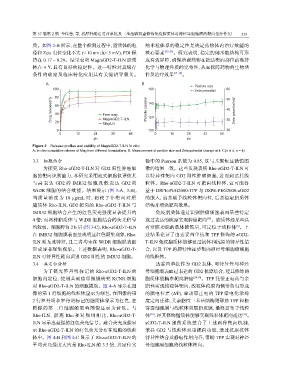
质。如图 2-B 所示,在整个检测过程中,脂质体的粒 纳米粒体系的稳定性是决定药物体内治疗效能的
径和 Zeta 电位变化不大 (< 10 nm 或< 5 mV),PDI 保 核心要素 [25−26] 。研究表明,稳定的纳米粒结构可形
持在 0.17 ~ 0.29。结果表明 Mag/aGD2-T-ILN 脂质 成有效屏障,确保所载药物在抵达靶向部位前维持
体在 4 ℃ 具有良好的稳定性。这一特性对其储存 化学与物理性质的完整性,从而保障药物的生物活
条件的确定及临床转化应用具有关键指导意义。 性及治疗效果 [27−28] 。
A B Particle size
100 160 Zeta potential 60
80
Drug released/% 60 Free mag Particle size/nm 140 40 Zeta potential/mV
50
40
120
Mag/aGD2-T-ILN
30
20
0 Mag/LN 100 20
0 12 24 36 48 0 14 28 42 56
t/h t/d
Figure 2 Release profiles and stability of Mag/aGD2-T-ILN in vitro
A: In vitro cumulative release of Mag from different formulations; B: Measurement of particle size and Zeta potential change at 4 ℃( x ± s, n = 4)
3.3 细胞结合 验中的 Pearson 系数为 0.85,这与共聚焦显微镜图
为探究 Rho-aGD2-T-ILN 对 GD2 阳性肿瘤细 像的结果一致。这些发现表明 Rho-aGD2-T-ILN 可
胞的靶向识别能力,本研究采用流式细胞仪评估其 以特异性靶向 GD2 阳性肿瘤细胞,进而到达其线
与 高 表 达 GD2 的 IMR32 细 胞 及 低 表 达 GD2 的 粒体。Rho-aGD2-T-ILN 可靶向线粒体,这可能得
WiDR 细胞的结合效能。结果显示 (图 3-A、3-B), 益于 DSPE-PEG2000-TPP 与 DSPE-PEG2000-aGD2
当质量浓度为 10 μg/mL 时,相较于非靶向对照 的嵌入,前者赋予线粒体靶向性,后者稳定脂质体
脂质体 Rho-ILN,GD2 靶向的 Rho-aGD2-T-ILN 与 结构并增强靶向效果。
IMR32 细胞结合产生的红色荧光强度显著提升约 免疫脂质体通过识别肿瘤细胞表面某些特定
4 倍;而两种脂质体与 WiDR 细胞结合的荧光信号 或过表达的抗原实现肿瘤靶向 。脂质体经某些具
[29]
均较弱。细胞孵育 2 h 后 (图 3-C),Rho-aGD2-T-ILN 有穿膜功能的载体修饰后,可定位于线粒体 。上
[8]
在 IMR32 细胞膜表面呈现明显红色凝集现象,Rho- 述结果论证了由达妥西单抗和 TPP 修饰的 aGD2-
ILN 则无此特征,且二者均未在 WiDR 细胞膜表面 T-ILN 免疫脂质体能够通过抗体和抗原的特异性结
形成显著凝集现象。上述数据表明,Rho-aGD2-T- 合,以及 TPP 跨膜特性逐步靶向神经母细胞瘤细胞
ILN 可特异性靶向识别 GD2 阳性的 IMR32 细胞。 的线粒体。
3.4 共定位分析 达妥西单抗作为 GD2 抗体,可特异性与神经
为了研究罗丹明标记的 Rho-aGD2-T-ILN 的 母细胞瘤表面过表达的 GD2 抗原结合,经其修饰的
细胞内定位,使用共聚焦显微镜研究 KCNR 细胞 脂质体能精准靶向肿瘤 [26,30] 。TPP 凭借正电荷与亲
对 Rho-aGD2-T-ILN 的细胞摄取。图 4-A 显示在图 脂性实现线粒体靶向:线粒体内膜内侧带负电形成
像的第 1 行细胞的线粒体显示为绿色,在图像的第 的膜电位差 (ΔΨ),驱动带正电的 TPP 沿电化学梯
2 行罗丹明和罗丹明标记的脂质体显示为红色,在 度定向迁移;其亲脂性三苯基结构则帮助 TPP 轻松
图像的第三行细胞的重叠图像显示为黄色。与 穿透细胞膜与线粒体双层脂质膜,最终富集于线粒
Rho-ILN、游离 Rho 和对照组相比,Rho-aGD2-T- 体 ,经其修饰脂质体能够实现线粒体靶向递送 。
[31]
[10]
ILN 显示出最强的红色荧光信号。融合荧光成像显 aGD2-T-ILN 递药系统整合了上述两种靶向机制,
示 Rho-aGD2-T-ILN 的红色荧光分布在细胞的线粒 兼具 GD2 与线粒体双重靶向功能,通过抗原抗体
体中。图 4-B 和图 4-C 显示了 Rho-aGD2-T-ILN 的 特异性结合及静电作用内吞,借助 TPP 实现对神经
平均荧光强度大约是 Rho-ILN 的 3.5 倍,共定位实 母细胞瘤细胞的线粒体靶向。