Page 86 - 《中国药科大学学报》2026年第2期
P. 86
212 学报 Journal of China Pharmaceutical University 2026, 57(2): 206 − 214 第 57 卷
定性,考察 LL-PTP/ZnPc 纳米粒在 96 h 内的粒径稳 性,可满足临床中对注射剂型药物的稳定性要求。
定性。结果如图 5-C 所示,将 LL-PTP/ZnPc 纳米粒溶 48 h 后粒径小幅度增加,说明 LL-PTP/ZnPc 纳米粒
液在室温条件下放置,48 h 内其平均粒径稳定在 水溶液在室温长时间放置可能发生部分降解,长期
80~90 nm,表明该纳米粒在 48 h 内具有优异的稳定 保存应制备成冻干制剂。
A B C
50 Tumor homogenates 50 Tumor homogenates 150
Serum 40 Serum
Degradation ratio/% 30 Release ratio/% 30 Size/nm 100
40
20
20
10
0 10 0 50
12 24 36 48 60 12 24 36 48 60 0 2 4 6 8 10 12 24 48 72 96
t/h t/h t/h
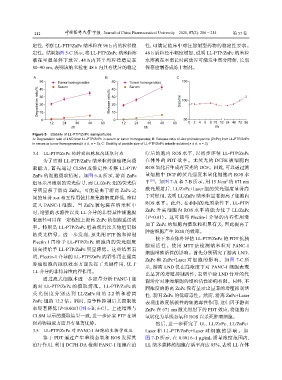
Figure 5 Stability of LL-PTP/ZnPc nanoparticles
A: Degradation ratio of LND from LL-PTP/ZnPc in serum or tumor homogenates; B: Release ratio of zinc phthalocyanine (ZnPc) from LL-PTP/ZnPc
in serum or tumor homogenates( x ± s, n = 3); C: Stability of particle size of LL-PTP/ZnPc micelle solution( x ± s, n = 3)
3.4 LL-PTP/ZnPc 的肿瘤细胞靶向摄取行为 疗后的胞内 ROS 水平,以初步评估 LL-PTP/ZnPc
为了监测 LL-PTP/ZnPc 纳米粒的肿瘤靶向摄 在体外的 PDT 效率。无荧光的 DCFH 被细胞内
取能力,首先通过 CLSM 成像定性考察 LL-PTP/ ROS 氧化后生成有荧光的 DCF。因此,可以通过测
ZnPc 的细胞摄取情况。如图 6-A 所示,游离 ZnPc 量细胞中 DCF 的荧光强度来量化细胞内 ROS 水
[18]
组显示出微弱的荧光信号,而 LL/ZnPc 组的荧光信 平 。如图 7-A 和 7-B 所示,用 15 J/cm 的 2 671 nm
号明显强于游离 ZnPc。可能是由于游离 ZnPc 之 激光照射后,LL/ZnPc+Laser 组的荧光强度显著高
间的显著 π-π 相互作用使其聚集溶解度降低,难以 于对照组,表明 LL/ZnPc 纳米粒显著提高了细胞内
进入 PANC-1 细胞。当 ZnPc 被包裹在纳米粒中 ROS 水平。此外,在相同的光照条件下,LL-PTP/
ZnPc 升高细胞内 ROS 水平的能力优于 LL/ZnPc
时,增强的水溶性以及 LL 介导的非特异性细胞摄
(P<0.01)。这可能与 Plectin-1 介导的内吞作用增
取途径可以在一定程度上提高 ZnPc 的细胞递送效
加了 ZnPc 的细胞内摄取和积累有关,因此提高了
率。特别是 LL-PTP/ZnPc 组表现出比其他组更强
肿瘤细胞产生 ROS 的效率。
的荧光信号。进一步发现,预先用 PTP 饱和抑制
接下来在体外评估 LL-PTP/ZnPc 的 PDT 抗胰
Plectin 1 再给予 LL-PTP/ZnPc 细胞内的荧光强度
腺癌活性。使用 MTT 法检测纳米粒对 PANC-1
较直接给予 LL-PTP/ZnPc 明显降低。这些结果表
细胞增殖活性的影响。首先分别研究了游离 LND、
明,Plectin-1 介导的 LL-PTP/ZnPc 内吞作用在提高
ZnPc 和 ZnPc+Laser 对细胞的影响。如图 7-C 所
肿瘤细胞的摄取效率方面发挥了关键作用,优于
示,游离 LND 仅在高浓度下对 PANC-1 细胞表现
LL 介导的非特异性内吞作用。
出显著的增殖抑制活性,表明单独 LND 针对的代
通过流式细胞术进一步定量分析 PANC-1 细
谢治疗对肿瘤细胞的增殖活性影响有限。同样,不
胞对 LL-PTP/ZnPc 的摄取情况。LL-PTP/ZnPc 的 同浓度的游离 ZnPc 没有显示出显著的增殖抑制活
荧 光 强 度 分 别 达 到 LL/ZnPc 组 的 2.2 倍 和 游 离 性,表明 ZnPc 的低暗毒性。然而,游离 ZnPc+Laser
ZnPc 组的 12.2 倍。同时,竞争性抑制后其摄取效 表现出浓度依赖性的细胞毒性作用,这归因于游离
率显著降低(P<0.001)(图 6-B,6-C)。上述结果与 ZnPc 在 671 nm 激光照射下的 PDT 效应,将细胞内
CLSM 显示的摄取结果一致,进一步证实 PTP 在增 氧转化为单线态氧和 ROS 以杀死肿瘤细胞。
强药物摄取方面具有显著优势。 然后,进一步研究了 LL、LL/ZnPc、LL/ZnPc+
3.5 LL-PTP/ZnPc 对 PANC-1 细胞的生物学效应 Laser 和 LL-PTP/ZnPc+Laser 对 细 胞 的 影 响 。 如
鉴于 PDT 通过产生单线态氧和 ROS 发挥其 图 7-D 所示,在 0.001 6~1 μg/mL 质量浓度范围内,
治疗作用,利用 DCFH-DA 检测 PANC-1 细胞在治 LL 纳米载体的细胞存活率高达 85%,表明 LL 在体