Page 127 - 《中国药科大学学报》2026年第2期
P. 127
许译尹,等:吲哚布芬通过抑制 NF-κB/Caspase-1/GSDMD 通路减轻脑缺血再灌注损伤的作用
第 57 卷第 2 期 与机制研究 253
A
Control OGD/R Aspirin (100 μmol/L) Indobufen (200 μmol/L)
50 μm 50 μm 50 μm 50 μm
B C TXB 2 6-keto-PGF 1 α
1.2 200 ## 500
1.0 150 ## ** ** * 400
Cell viability/% 0.6 ## ** ** Concentration of TXB 2 /(pg/mL) 100 300 Concentration of 6-keto-PGI 1 α/(pg/mL)
0.8
200
0.4
0.2 50 100
0 0 0
Control OGD/R Aspirin Indobufen Control OGD/R Aspirin Indobufen
(100 μmol/L) (200 μmol/L) (100 μmol/L) (200 μmol/L)
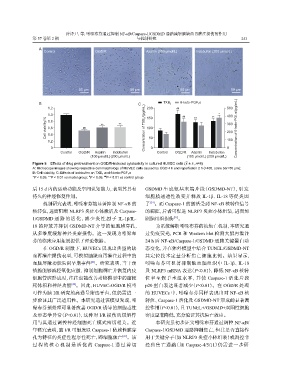
Figure 5 Effects of drug pretreatment on OGD/R-induced cytotoxicity in cultured HUVEC cells ( x ± s, n=8)
A: Microscope images showing respective cell morphology of HUVEC cells caused by OGD 4 h and reperfusion 2 h (×400, scale bar=50 μm);
B: Cell viability; C: Effects of indobufen on TXB 2 and 6-keto-PGF 1 α
##
#
*P < 0.05, **P < 0.01 vs model group; P < 0.05, P < 0.01 vs control group
后 15 d 内的运动功能及空间认知能力,表明其具有 GSDMD 生成氨基末端片段(GSDMD-NT),引发
持久的神经修复作用。 细胞膜通透性改变并释放 IL-1β、IL-18 等促炎因
机制研究表明,吲哚布芬能显著抑制 NF-κB 的 子 。而 Caspase-1 的激活受到 NF-κB 核转位信号
[24]
核转位,进而阻断 NLRP3 炎症小体激活及 Caspase- 的调控,后者可促进 NLRP3 炎症小体组装,进而加
[25]
1/GSDMD 通路的活化,减少炎性因子 IL-1β/IL- 剧脑组织损伤 。
18 的释放并抑制 GSDMD-NT 介导的细胞膜穿孔, 为系统解析吲哚布芬的抗焦亡机制,本研究通
从多维度缓解神经炎症损伤。这一发现为吲哚布 过免疫荧光,PCR 和 Western blot 检测大鼠再灌注
芬的临床应用拓展提供了理论依据。 24 h 后 NF-κB/Caspase-1/GSDMD 通路关键蛋白动
在 OGD/R 刺激下,HUVECs 展现出典型的缺 态变化,并在体外模型中结合 TUNEL/GSDMD-NT
血再灌注损伤表型,可模拟脑缺血再灌注过程中的 共定位技术定量分析焦亡细胞比例。结果显示,
[21]
血脑屏障功能失调早期事件 。研究表明,当干预 吲哚布芬可显著抑制缺血脑组织中 IL-1β、IL-18
措施能够减轻氧化应激、抑制细胞凋亡并恢复内皮 及 NLRP3 mRNA 表达(P<0.01),降低 NF-κB 核转
细胞管腔形成时,往往也能改善动物模型中的脑梗 位率至假手术组水平,并使 Caspase-1 活化片段
[22]
死体积和神经功能 。因此,HUVEC-OGD/R 模型 p20 蛋白表达显著减少(P<0.01)。在 OGD/R 处理
可作为脑 I/R 研究的高通量筛选平台,但仍需进一 的 HUVECs 中,吲哚布芬同样表现出对 NF-κB 核
步验证其广泛适用性。本研究通过该模型发现,吲 转位、Caspase-1 活化及 GSDMD-NT 形成的显著调
哚布芬预处理可显著改善 OGD/R 诱导的细胞毒性 控作用(P<0.01),且 TUNEL+/GSDMD+双阳性细胞
及形态学异常(P<0.01),这种对 I/R 损伤的缓解作 密度显著降低,充分验证其抗焦亡效应。
用与其通过调控神经细胞死亡模式密切相关。近 本研究虽初步证实吲哚布芬通过调控 NF-κB/
年研究表明,脑 I/R 可触发以 Caspase-1 依赖性膜穿 Caspase-1/GSDMD 通路抑制焦亡,但其是否直接作
孔为特征的炎症性程序性死亡,即细胞焦亡 。该 用于关键分子(如 NLRP3 炎症小体组装)或调控非
[23]
过 程 的 核 心 机 制 是 活 化 的 Caspase-1 通 过 剪 切 经典焦亡通路(如 Caspase-4/5/11)仍需进一步研