Page 63 - 《中国药科大学学报》2026年第1期
P. 63
涂佳卉,等:LC-MS/MS 法测定小型猪血浆中泰妙菌素浓度及其在不同制剂
第 57 卷第 1 期 药代动力学研究中的应用 57
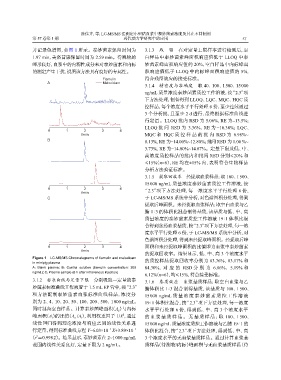
并记录色谱图,如图 1 所示。泰妙菌素保留时间为 3.1.3 残 留 在对定量上限样本进行检测后,空
1.97 min,美洛昔康保留时间为 2.59 min。待测物的 白样品中泰妙菌素峰面积响应值低于 LLOQ 中泰
峰形良好,血浆中的内源性成分未对泰妙菌素和内标 妙菌素峰面积响应值的 20%,空白样品中内标峰面
的测定产生干扰,说明该方法具有良好的专属性。 积响应值低于 LLOQ 中内标峰面积响应值的 5%,
Tiamulin
符合残留效应的接受标准。
A Meloxiciam
3.1.4 精密度与准确度 取 40、100、1 500、15 000
ng/mL 质量浓度泰妙菌素质控工作溶液,按“2.3”项
下方法处理,制备得到 LLOQ、LQC、MQC、HQC 质
控样品,每个浓度水平平行处理 6 份,至少连续通过
3 个分析批,且至少 2 d 进行,最终根据标准曲线进
行定量。LLOQ 批内 RSD 为 5.06%,RE 为–13.5%;
LLOQ 批 间 RSD 为 3.36%, RE 为 −10.38%; LQC、
0 1 2 3 4
t/min MQC 和 HQC 质 控 样 品 的 批 内 RSD 为 6.98%~
B
8.13%,RE 为−14.00%~12.80%;批间 RSD 为 1.00 %~
3.73%,RE 为−14.00%~14.67%。定量下限及低、中、
高浓度质控样品的批内和批间 RSD 分别≤20% 和
≤15%(n=6),RE 均在±15% 内,表明符合生物样品
分析方法验证标准。
3.1.5 提取回收率 经提取血浆样品:取 100、1 500、
15 000 ng/mL 质量浓度泰妙菌素质控工作溶液,按
0 1 2 3 4 “2.3”项下方法处理,每一浓度水平平行处理 6 份,
t/min
C 于 LC-MS/MS 系统中分析,对色谱图积分处理,得到
提取后峰面积。未经提取血浆样品:取空白血浆与乙
腈 1∶3 的体积比混合制得基质,该基质与低、中、高
质量浓度的泰妙菌素质控工作溶液 19∶1 体积比混
合得到含药血浆基质,按“2.3”项下方法处理,每一浓
度水平平行处理 6 份,于 LC-MS/MS 系统中分析,对
色谱图积分处理,得到未经提取峰面积。经提取后峰
0 1 2 3 4 面积和未经提取峰面积的比值即为血浆中泰妙菌素
t/min
的提取回收率。结果显示,低、中、高 3 个浓度水平
Figure 1 LC-MS/MS Chromatograms of tiamulin and meloxicam
in minipig plasma 的质控样品提取回收率分别为 83.76%、83.17% 和
A: Blank plasma; B: Control solution (tiamulin concentration: 200 84.30%, 对 应 的 RSD 分 别 为 6.86%、 5.19% 和
ng/mL); C:Plasma sample (6 h after intravenous injection)
6.12%(n=6),均≤15%,符合接受标准。
3.1.2 标准曲线与定量下限 分别吸取一定量的泰 3.1.6 基质效应 血浆基质样品:取空白血浆与乙
妙菌素标准曲线工作液置于 1.5 mL EP 管中,按“2.3” 腈体积比 1∶3 混合制得基质,该基质与 100、1 500、
项方法配制泰妙菌素血浆标准曲线样品,浓度分 15 000 ng/mL 质 量 浓 度 泰 妙 菌 素 质 控 工 作 溶 液
别为 2、4、10、20、50、100、200、500、1 000 ng/mL, 19∶1 体积比混合,按“2.3”项下方法处理,每一浓度
同时制备空白样品。计算泰妙菌峰面积(A )与内标 水平平行处理 6 份,得到低、中、高 3 个浓度水平
s
峰面积(A )的比值(A /A ),利用权重因子 1/X ,通过 的 血 浆 基 质 样 品 。 无 基 质 样 品 : 取 100、 1 500、
2
i s i
线性回归得到理论浓度与响应之间的线性关系进 15 000 ng/mL 质量浓度质控工作溶液与乙腈 19∶1 的
行定量,得到标准曲线方程 Y=6.03×10 X+3.89×10 −3 体积比混合,按“2.3”项下方法处理,得到低、中、高
−3
(r =0.998 2)。结果显示,泰妙菌素在 2~1 000 ng/mL 3 个浓度水平的无血浆基质样品。通过计算血浆基
2
范围内线性关系良好,定量下限为 2 ng/mL。 质样品(待测物/内标)峰面积与无血浆基质样品(待