Page 102 - 《中国药科大学学报》2026年第1期
P. 102
96 学报 Journal of China Pharmaceutical University 2026, 57(1): 90 − 97 第 57 卷
A B Control
MFN2 * DCM
2.5 * * * Atr-I low-dose
* * Atr-I high-dose
Captopril
DRP1 2.0 * * * * * Atr-I high-dose+DMXAA
Protein relative expression * * * * * *
cGAS * * * * * * * * * *
STING 1.5 * * * * * * * *
*
IFN-β 1.0 * * * * * * * *
* *
CXCL10 0.5 * * *
IL-6 0
GAPDH MFN2 DRP1 cGAS STING IFN-β CXCL10 IL-6
1 2 3 4 5 6
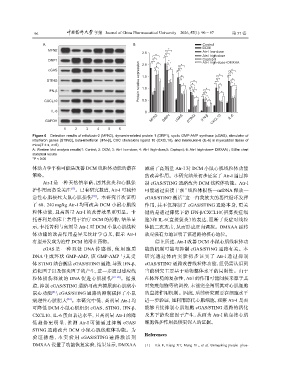
Figure 6 Detection results of mitofusin-2 (MFN2), dynamin-related protein 1 (DRP1), cyclic GMP-AMP synthase (cGAS), stimulator of
interferon genes (STING), beta-interferon (IFN-β), CXC chemokine ligand 10 (CXCL10), and interleukin-6 (IL-6) in myocardial tissue of
mice( x ± s, n=6)
A: Western blot analysis results(1: Control; 2: DCM; 3: Atr-I low-dose; 4: Atr-I high-dose;5: Captopril; 6: Atr-I high-dose+ DMXAA) ; B:Bar chart
statistical results
*P < 0.05
体动力学平衡可能是改善 DCM 线粒体功能的潜在 减弱了高剂量 Atr-I 对 DCM 小鼠心肌线粒体功能
策略。 的改善作用。本研究结果初步证实了 Atr-I 通过抑
Atr-I 是一种天然倍半萜,因其抗炎和心肌保 制 cGAS/STING 通路改善 DCM 线粒体功能。Atr-I
护作用而备受关注 。已有研究报道,Atr-I 可减轻 可能通过直接干预“线粒体损伤—mtDNA 释放—
[17]
急性心肌梗死大鼠心肌损伤 。本研究首次证明 cGAS/STING 激活”这一自我放大的恶性循环发挥
[18]
了 60、240 mg/kg Atr-I 均可改善 DCM 小鼠心肌线 作用,其不仅抑制了 cGAS/STING 通路本身,更关
粒体功能,且高剂量 Atr-I 的改善效果更明显。卡 键的是通过降低下游 IFN-β/CXCL10(招募炎症细
托普利是临床上常用于治疗 DCM 的药物,结果显 胞)和 IL-6(直接促炎)的表达,阻断了炎症对线粒
示,卡托普利与高剂量 Atr-I 对 DCM 小鼠心肌线粒 体的二次攻击,从而形成正向调控。DMXAA 逆转
体功能的改善作用差异无统计学意义,提示 Atr-I 效应强有力地证明了该通路的核心地位。
有望开发成为治疗 DCM 的潜在药物。 综上所述,Atr-I 改善 DCM 小鼠心肌线粒体功
cGAS 是 一 种 双 链 DNA 传 感 器 , 使 用 胞 质 能的机制可能与抑制 cGAS/STING 通路有关。本
DNA 生成环状 GMP-AMP,该 GMP-AMP 与其受 研 究 通 过 体 内 实 验 初 步 证 实 了 Atr-I 通 过 抑 制
体 STING 结合激活 cGAS/STING 通路,导致 IFN-β、 cGAS/STING 通路改善线粒体功能,但仍需认识到
趋化因子以及促炎因子的产生,进一步通过感应线 当前研究主要基于动物整体水平的局限性。由于
粒体损伤释放的 DNA 促进心肌损伤 [19−20] 。据报 在体环境的复杂性,AtrI 的作用可能间接来源于其
道,抑制 cGAS/STING 通路可改善糖尿病心肌病小 对免疫细胞等的调控,未能完全阐明其对心肌细胞
[21]
鼠心功能 ;cGAS/STING 通路的抑制减轻了小鼠 的直接作用机制。因此,后续研究需要在细胞水平
病理性心脏肥大 。本研究中低、高剂量 Atr-I 均 进一步验证,如利用原代心肌细胞,观察 Atr-I 是否
[22]
可降低 DCM 小鼠心肌组织 cGAS、STING、IFN-β、 能够直接抑制心肌细胞 cGAS/STING 通路的活化
CXCL10、IL-6 蛋白表达水平,且高剂量 Atr-I 的降 及其下游炎症因子产生,从而为 Atr-I 的直接心肌
低趋势更明显,推测 Atr-I 可能通过抑制 cGAS/ 细胞保护作用提供更深入的证据。
STING 通路改善 DCM 小鼠心肌线粒体功能。为
验 证 猜 想 , 本 实 验 用 cGAS/STING 通 路 激 活 剂 References
DMXAA 设置了功能恢复实验,结果显示,DMXAA [1] Lin F, Liang XT, Meng YL, et al. Unmasking protein phos-