Page 79 - 《中国药科大学学报》2025年第5期
P. 79
第 56 卷第 5 期 栾亚萁,等:医用臭氧对脓毒症肾损伤的治疗作用及其机制 611
Macrophage
Renal tubule Renal tubule
TNF-α
IL-1β
p53
PAR-2 LPS Ozone
PAR-2
NETs
MP-TF
Renal tubular epithelial cell
O 3
P
AMPK
LPS
Microvessel
SR-A1
NETs NETs MP-TF
Macrophage MP-TF
Macrophage
Neutrophil
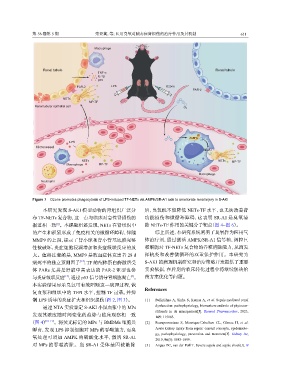
Figure 7 Ozone promotes phagocytosis of LPS-induced TF-NETs via AMPK/SR-A1 axis to ameliorate renal injury in S-AKI
本研究发现 S-AKI 模型动物的肾组织广泛分 后,臭氧既不能降低 NETs-TF 水平,也无法改善肾
布 TF-NETs 复合物,这一点与临床对急性肾损伤的 功能损伤和微循环障碍,这表明 SR-A1 是臭氧清
报道相一致 。本课题组还发现,NETs 在肾组织中 除 NETs-TF 作用的关键分子靶点(图 4~图 6)。
[8]
的产生和积累形成了免疫相关的微循环障碍,伴随 综上所述,本研究系统阐明了臭氧作为医用气
MMP9 的上调,提示了肾小球和肾小管基底膜完整 体治疗剂,通过激活 AMPK/SR-A1 信号轴,调控巨
性被破坏,炎症细胞浸润增加和炎症级联反应的放 噬细胞对 TF-NETs 复合物的吞噬清除能力,从而发
大。值得注意的是,MMP9 是败血症休克患者 28 d 挥抗炎和改善微循环的双重保护作用。本研究为
[14]
病死率的独立预测因子 ,TF 的配体蛋白酶激活受 S-AKI 的病理机制研究和治疗策略开发提供了重要
体 PARs 尤其是肾脏中高表达的 PAR-2 亚型也参 实验依据,在后期的临床转化过程中将继续解决给
与炎症级联反应 ,通过 p53 信号诱导肾细胞凋亡 。 药方案优化等问题。
[5]
[15]
本实验结果显示臭氧可有效阻断这一病理过程,恢
复血浆和组织中的 TFPI 水平,控制 TF 过载,并抑 References
制 LPS 诱导的炎症扩大和组织损伤(图 2,图 3)。 [1] Balkrishna A, Sinha S, Kumar A, et al. Sepsis-mediated renal
通过 NTA 实验鉴定 S-AKI 小鼠血浆中的 MPs dysfunction: pathophysiology, biomarkers and role of phytocon-
stituents in its management[J]. Biomed Pharmacother, 2023,
发现其浓度随时间变化的趋势与临床观察相一致
165: 115183.
(图 4) [16−17] 。将荧光标记的 MPs 与 BMDMs 细胞共 [2] Peerapornratana S, Manrique-Caballero CL, Gómez H, et al.
孵育,发现 LPS 抑制细胞对 MPs 的吞噬能力,而臭 Acute kidney injury from sepsis: current concepts, epidemiolo-
gy, pathophysiology, prevention and treatment[J]. Kidney Int,
氧处理可增加 AMPK 的磷酸化水平,激活 SR-A1
2019, 96(5): 1083-1099.
对 MPs 的吞噬清除。当 SR-A1 受体基因被敲除 [3] Angus DC, van der Poll T. Severe sepsis and septic shock[J]. N