Page 50 - 《中国药科大学学报》2026年第1期
P. 50
44 学报 Journal of China Pharmaceutical University 2026, 57(1): 34 − 45 第 57 卷
结果显示先导物 4 的 6 种性质均不满足要求,而化 是,化合物 25 不太可能为 P-糖蛋白(P-glycoprotein,
合物 25 只有 TPSA 和饱和度不满足要求,这表明化 P-gp)底物,并且表现出较低的药物-药物相互作用的
合物 25 的透膜性质要明显优于先导物 4,有望具有 潜力。药物相似性是药物开发的一个重要方面,用
更优的口服生物利用度。先导物 4 和化合物 25 被 于评估分子成为口服药物的潜力。类药性五规则
预测具有低水平的胃肠(gastrointestinal, GI)吸收,无 (Lipinski 规则)是目前常用的类药性评价指标 [23−24] ,
通过血脑屏障(blood-brain barrier, BBB)的可能性, 先导物 4 是不满足该规则的,而化合物 25 被预测
但还是需要开展实验研究来验证这些预测。有趣的 在 Lipinski 规则中具有较优类药性(表 4)。
Table 4 Molecular properties of compounds 25 calculated by SwissADME software
Fraction GI BBB P-gp
Compd. XLOGP3 M r TPSA lgS RB Lipinski
C sp 3 absorption permeable substrate
25 0.44 365.39 177.68 −2.55 0.25 7 Low No No Yes
4 6.91 632.75 193.03 −8.05 0.19 13 Low No No No
XLOGP3: Tool for predicting the octanol/water partition coefficient of chemical substances; TPSA: Topological polar surface area; S: Solubility; RB:
Number of rotatable bonds; GI: Gastrointestinal; BBB: Blood-brain barrier; P-gp: P-glycoprotein; Lipinski: Drug-likeness evaluation indices
6 细胞毒性评价 25 具有微摩尔级的抗肿瘤活性(IC = 28.09 ± 1.04
50
μmol/L)(图 6-A)。本研究进一步测试了化合物
基于酶水平的 LDHA 抑制活性的研究结果,
25 对正常 HUVEC 细胞的细胞毒性以评估其安全
化合物 25 具有最优的 LDHA 抑制活性,因此采用 性。结果显示,在所测试的浓度下,HUVEC 细胞存
MTT 比色法评估其在体外对胰腺癌 Mia PaCa-2 细 活率均大于 85%,表明其对正常细胞无明显毒性作
胞的抗肿瘤细胞增殖活性。结果显示,化合物 用,具有良好的安全性(图 6-B)。
A B
100 150
Inhibition/% 50 Cell viability/% 100
50
IC 50 =28.09±1.04 μmol/L
0 0
−1 0 1 2 3 300 100 33 11
lgc c/(μmol/L)
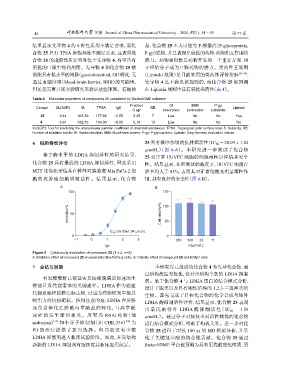
Figure 6 Cytotoxicity evaluation of compound 25 ( x ± s, n=3)
A: Inhibitory effect of compound 25 on pancreatic Mia-PaCa-2 cells; B: Viability effect of compound 25 on HUVEC cells
7 总结与展望 本研究以已报道的化合物 4 为先导化合物,通
过结构改造与优化,设计出结构全新的 LDHA 抑制
有氧糖酵解已被证实是癌细胞满足加速的生
剂。基于化合物 4 与 LDHA 蛋白的结合模式分析,
物能量及代谢需求的关键途径。LDHA 作为癌症
设计了脲类以及具有刚性结构的 1,2,3-三氮唑类衍
代谢重编程的核心标志物,已成为药物研发中极具
生物。首先完成了目标化合物的化学合成与体外
吸引力的抗癌靶标。值得注意的是,LDHA 在肝脏 LDHA 酶抑制活性评价,结果显示,化合物 25 表现
还负责催化乙醛酸向草酸盐的转化,与高草酸 出 最 优 的 体 外 LDHA 酶 抑 制 活 性 ( IC = 1.59
50
尿 症 的 发 生 密 切 相 关 。 肝 靶 向 RNAi 药 物 ( 如 μmol/L)。通过分子对接技术对活性较优的化合物
nedosiran) [16] 和小分子抑制剂(如 CHK-336) [14] 为 进行结合模式分析,明确了构效关系。进一步对化
PH 的治疗提供了新兴选择。但目前仅有少数 合物 25 进行了时长 100 ns 的 MD 模拟分析,并量
LDHA 抑制剂进入临床试验阶段。因此,开发结构 化了关键氨基酸的结合能贡献。化合物 25 通过
新颖的 LDHA 抑制剂有望拓宽其临床应用前景。 SwissADME 平台被预测为具有更优的理化性质,更