Page 49 - 《中国药科大学学报》2026年第1期
P. 49
第 57 卷第 1 期 邴天德,等:乳酸脱氢酶 A 抑制剂的设计、合成与生物活性 43
的能量贡献要弱于先导物 4,这进一步阐释了化合 参数 。本研究中,使用 SwissADME 在线平台预
[21]
物 25 在 LDHA 抑制活性方面弱于先导物 4 的原因。 测评估化合物 25 的理化性质、药代动力学性质和药
物相似性。药物穿透细胞膜并在体内运输的能力
5 理化性质以及药代动力学参数模拟预测
与 6 种性质密切相关,包括亲脂性(XLOGP3 介于
分子固有的理化性质以及药代动力学特征评估 −0.7 和 5.0 之间),相对分子质量(M 介于 150 和
r
是药物发现和开发的一个重要方面,包括与药物的 500 之间 ),拓扑极性表面积(TPSA 介于 20 Å 和
2
3
2
吸收、分布、代谢、排泄和毒性(absorption, distribution, 130 Å 之间),溶解度(lgS≤6),饱和度(sp 杂化中的
metabolism, excretion and toxicity, ADMET)相关的 碳分数≥0.25)和分子柔性(可旋转键≤9) 。预测
[22]
A Arg168 B Arg168 His192
His192
Compound 25 Compound 4 Glu191
Glu191
Asp140
Thr247
Asp140 Thr247 Arg105
Arg105
Ile141
NADH NADH
Asn137 Asn137 Pro138
Pro138 Ile141
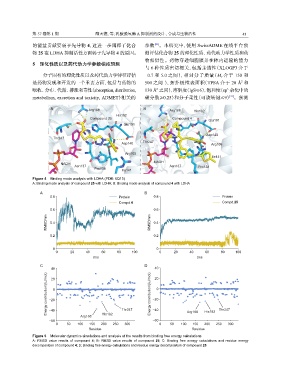
Figure 4 Binding mode analysis with LDHA (PDB: 6Q13)
A: Binding mode analysis of compound 25 with LDHA; B: Binding mode analysis of compound 4 with LDHA
A B
0.8 Protein 0.8 Protein
Compd.4 Compd.25
0.6 0.6
RMSD/nm 0.4 RMSD/nm 0.4
0.2 0.2
0 0
0 20 40 60 80 100 0 20 40 60 80 100
t/ns t/ns
C D
40 40
Energy contribution/(kJ/mol) −20 Energy contribution/(kJ/mol) −20 0
20
20
0
−40
−60
−60 Arg168 His192 Thr247 −40 Arg168 His192 Thr247
0 50 100 150 200 250 300 0 50 100 150 200 250 300
Residue Residue
Figure 5 Molecular dynamics simulations and analysis of the results from binding free energy calculations
A: RMSD value results of compound 4; B: RMSD value results of compound 25; C: Binding free energy calculations and residue energy
decomposition of compound 4; D: Binding free energy calculations and residue energy decomposition of compound 25