Page 44 - 《中国药科大学学报》2025年第5期
P. 44
576 学报 Journal of China Pharmaceutical University 2025, 56(5): 572 − 582 第 56 卷
A B 150 HepG2 C 100 P=0.001 2
HCC-LM3
MHCC-97H
r =0.846 2
2
Hep3B SMMC-7721 Bel-7402 HCC-LM3 HepG2 SK-Hep-1 MHCC-97L 100 Bel-7402 80
SMMC-7721
60
Hep3B
AKR1C3 Relative cell viability/% 50 SK-Hep-1 IC 50 /(mmol/L) 40
β-actin MHCC-97H 20
MHCC-97L
0
0 20 40 60 0 0 1 2 3 4
c(metformin)/(mmol/L) AKR1C3/β-actin
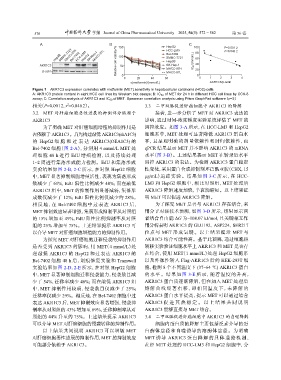
Figure 1 AKR1C3 expression correlates with metformin (MET) sensitivity in hepatocellular carcinoma (HCC) cells
A: AKR1C3 protein content in eight HCC cell lines by Western blot assays; B: IC 50 of MET for 24 h in different HCC cell lines by CCK-8
assay; C: Correlation analysis of AKR1C3 and IC 50 of MET. Spearman correlation analysis using Prism GraphPad software (n=3)
相关(P=0.001 2,r =0.846 2)。 3.3 二甲双胍促进肝癌细胞中 AKR1C3 的降解
2
3.2 MET 对肝癌细胞恶性进展的抑制部分依赖于 接着,进一步分析了 MET 对 AKR1C3 表达的
AKR1C3 影响,通过时间-浓度梯度实验系统评估了 MET 的
为了明确 MET 对肝癌细胞增殖的抑制作用是 调控效应。如图 3-A 所示,在 HCC-LM3 和 HepG2
否依赖于 AKR1C3。首先构建敲低 AKR1C3(shA1C3) 细胞系中,MET 处理可显著降低 AKR1C3 蛋白水
的 HepG2 细 胞 和 过 表 达 AKR1C3(OEA1C3) 的 平,且呈现明确的剂量依赖性和时间依赖性,而
Bel-7402 细胞(图 2-A),分别用 4 mmol/L MET 处 qPCR 结果显示 MET 并不影响 AKR1C3 的 mRNA
理细胞 48 h 进行 EdU 增殖检测,以及持续处理 水平(图 3-B)。上述结果提示 MET 在转录后水平
1~2 周进行集落形成能力检测。EdU 和集落形成 调控 AKR1C3 的表达。为检测 AKR1C3 蛋白稳定
实验结果如图 2-B,2-C 所示,在对照 HepG2 细胞 性变化,采用蛋白合成抑制剂环己酰亚胺(CHX,15
中,MET 显著抑制细胞增殖活性,表现为集落形成 μg/mL)追踪实验。结果如图 3-C 所示,在 HCC-
数减少了 61%,EdU 阳性比例减少 48%;而在敲低 LM3 和 HepG2 细胞中,相比对照组,MET 处理后
AKR1C3 组中,MET 的抑制作用显著减弱,集落形 AKR1C3 降解速度加快,半衰期缩短。以上结果证
成数仅减少了 12%;EdU 阳性比例仅减少约 28%。 明 MET 可以促进 AKR1C3 降解。
相反地,在 Bel-7402 细胞中过表达 AKR1C3 后, 为了探究 MET 是否与 AKR1C3 存在结合,采
MET 抑制效应显著增强,集落形成抑制率从对照组 用分子对接技术预测,如图 3-D 所示,结果显示两
的 15% 增加至 49%,EdU 阳性比例抑制率从对照 者结合自由能 ΔG 为–108.07 kJ/mol,且关键相互作
组的 25% 增加至 75%。上述结果提示 AKR1C3 可 用分析表明 AKR1C3 的 GLU192、ASP224、SER217
以介导 MET 对肝癌细胞增殖能力的抑制作用。 位点与 MET 形成氢键。以上结果提示 MET 与
为探究 MET 对肝癌细胞迁移侵袭的抑制作用 AKR1C3 结合可能性高。基于此预测,通过细胞热
是否受到 AKR1C3 的影响,用 MET(4 mmol/L)处 转移实验验证细胞水平上 AKR1C3 和 MET 是否存
理敲低 AKR1C3 的 HepG2 和过表达 AKR1C3 的 在结合,使用 MET(1 mmol/L)处理 HepG2 细胞系
Bel-7402 细胞 48 h 后,划痕修复实验和 Transwell 以及外源性转入 Flag-AKR1C3 后的 HEK-293T 细
实验结果如图 2-D,2-E 所示,在对照 HepG2 细胞 胞,检测 8 个不同温度下 (37~64 ℃) AKR1C3 蛋白
中,MET 显著抑制细胞迁移侵袭能力,侵袭数目减 的水平。结果如图 3-E 所示,随着温度的升高,
少了 54%,迁移率减少 46%;而在敲低 AKR1C3 组 AKR1C3 蛋白质逐渐降解,但在加入 MET 处理后
中,MET 抑制作用较弱,侵袭数目仅减少了 25%; 熔 解 曲 线 显 著 右 移 , 即 相 同 温 度 下 , 未 降 解 的
迁移率仅减少 29%。相反地,在 Bel-7402 细胞中过 AKR1C3 蛋白水平提高,提示 MET 可以通过结合
表达 AKR1C3 后,MET 抑制效应显著增强,侵袭抑 AKR1C3 促 进 其 热 稳 定 。 以 上 结 果 共 同 说 明
制率从对照组的 43% 增加至 69%,迁移抑制率从对 AKR1C3 能够直接与 MET 结合。
照组的 44% 升至约 75%。上述结果提示 AKR1C3 3.4 二甲双胍促进肝癌细胞中 AKR1C3 的自噬降解
可以介导 MET 对肝癌细胞的侵袭转移的抑制作用。 细胞内蛋白质的降解主要包括泛素介导的蛋
以上结果共同说明 AKR1C3 可以增敏 MET 白酶体途径和自噬诱导的溶酶体途径。为明确
对肝癌细胞恶性进展的抑制作用,MET 的抑制效应 MET 诱 导 AKR1C3 蛋 白 降 解 的 具 体 通 路 机 制 ,
可能部分依赖于 AKR1C3。 在经 MET 处理的 HCC-LM3 和 HepG2 细胞中,分