Page 18 - 《中国药科大学学报》2025年第5期
P. 18
550 学报 Journal of China Pharmaceutical University 2025, 56(5): 548 − 556 第 56 卷
复合物晶体结构为例来说明第二代 PRMT5 抑制剂
结合 PRMT5•MTA 复合物的结构基础。如图 2-A
所示,在 PRMT5•SAM 复合物中,Lys333 通过盐桥
MTAP 15%的癌症患者中出现
MTAP缺失 与 SAM 的羧基和 Glu435 形成较强的极性相互作
用,其中 Glu435 与底物 H4 蛋白的胍基形成盐桥。
MTA累积
当第二代 PRMT5 抑制剂结合到蛋白活性口袋中则
MTR-1P 第二代 引起了部分氨基酸侧链发生偏转,通过分析两个复
PRMT5
抑制剂 合物的叠合图(图 2-B)可以发现,F1 导致 Glu435
侧链向 SAM 口袋移动,从而导致 SAM 与 Glu435
PRMT5
之间的空间冲突。此外,F1 还促使 Lys333 远离
MAT2A
SAM 结合位点,破坏了 SAM 与 Lys333 之间的关
甲基化 SAM 键盐桥相互作用。因此,F1 虽然无法结合
基因转录、DNA复制、 甲硫氨酸 PRMT5•
基因组完整性缺陷 SAM 复合物,却能结合 PRMT5•MTA 复合物,这就
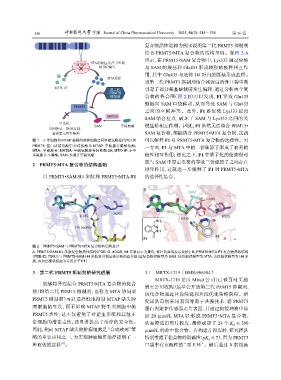
图 1 正常细胞和 MTAP 敲除的肿瘤细胞之间甲硫氨酸途径的区别 可以解释 F1 对 PRMT5•MTA 复合物的选择性。另
PRMT5:蛋白质精氨酸甲基转移酶 5;MTAP:甲硫腺苷磷酸化酶; 一方面,F1 与 MTA 中的二价硫原子形成了有利的
MTA: 甲硫腺苷;MAT2A:甲硫氨酸腺苷转移酶 2A;MTR-1P:5-甲
基硫腺苷-1-磷酸;SAM:S-腺苷甲硫氨酸 极性相互作用;相比之下,F1 中质子化的伯胺很可
能与 SAM 中带正电荷的等效三价硫原子之间存在
2 PRMT5∙MTA 复合物的结构基础
排斥作用,这就进一步解释了 F1 对 PRMT5•MTA
以 PRMT5•SAM-H4 多肽和 PRMT5•MTA-F1 的选择性结合。
A B
SAM
SAM
Clash
MTA
K333
E435 K333
E435
NH 2
H4 peptide N
NH
O F1
F1
图 2 PRMT5•SAM 与 PRMT5•MTA 复合物的结构差异
A:PRMT5•SAM-H4 多肽复合物晶体结构(PDB ID: 4GQB,H4 多肽显示为黄色,紫红色虚线表示盐桥);B:PRMT5•MTA-F1 复合物晶体结构
(PDB ID: 7S0U)与 PRMT5•SAM-H4 多肽复合物晶体结构的叠合图(蓝绿色棍状模型为 SAM,绿色棍状模型为 MTA,黄色棍状模型为 H4 多
肽,灰白色棍状模型为片段分子 F1)
3 第二代 PRMT5 抑制剂的研究进展 3.1 MRTX-1719(BMS-986504)
MRTX-1719 是由 Mirati 公司(已被百时美施
能够特异性结合 PRMT5•MTA 复合物的化合
贵宝公司收购)最早公开的第二代 PRMT5 抑制剂,
物(即第二代 PRMT5 抑制剂,也称为 MTA 协同型
该化合物通过片段筛选和片段优化策略获得。研
PRMT5 抑制剂)可以选择性地抑制 MTAP 缺失肿
究团队最初采用表面等离子共振技术,将 PRMT5
瘤细胞的生长,而不影响 MTAP 野生型细胞中的 蛋白固定在传感器芯片表面,并通过向缓冲液中添
PRMT5 活性,这不仅避免了对造血系统和其他正 加 20 μmol/L MTA 以形成 PRMT5•MTA 复合物,
常细胞的潜在毒性,还显著提高了治疗的安全性。 从而筛选市售片段库,最终确定了 24 个 K ≤ 500
d
因此,靶向 MTAP 缺失的肿瘤细胞是“合成致死”策 μmol/L 的命中化合物。在构建片段库时,研究团队
略的重要应用之一,为实现肿瘤精准治疗提供了一 特别考虑了化合物的弱碱性(pK ≤ 7),因为 PRMT5
a
种有效的途径 。 口袋中存在酸性的“双 E 环”。最后通过 X 射线晶
[17]