Page 80 - 《中国药科大学学报》2025年第4期
P. 80
476 学报 Journal of China Pharmaceutical University 2025, 56(4): 469 − 477 第 56 卷
A B Control PA PA+ PA+ PA+ PA+
ZLY16-5 ZLY16-10 ZLY16-20 simvastatin
150 DAPI
Cell viability/% 100 ** Nile red
50
DAPI
eMyHC
0
0 0.625 1.25 2.5 5 10 20 40 50
C D 2.0 PPARβ E 4 CPT-1a F 1.5 Myogenin **
CPT-1a 88 KDa 1.5 * ** 3 ## ** ** 1.0 *
PPARβ 52 KDa Relative protein expression 1.0 # * Relative protein expression 2 Relative protein expression
Myogenin 34 KDa 0.5 1 0.5
GAPDH 36 KDa 0 0 0
PA+ZLY16-10
PA+ZLY16-10
PA+simvastatin
PA+simvastatin
PA+simvastatin
PA+ZLY16-10
ZLY16 0 0 5 10 20 0 Control PA Control PA Control PA
PA − + + + + + PA+ZLY16-5 PA+ZLY16-20 PA+ZLY16-5 PA+ZLY16-20 PA+ZLY16-5 PA+ZLY16-20
Simvastatin − − − − − +
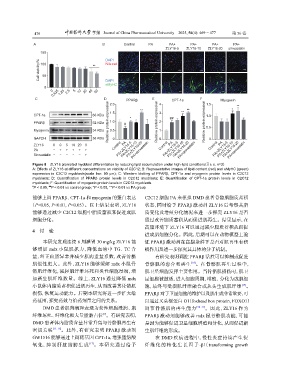
Figure 8 ZLY16 promoted myoblast differentiation by reducing lipid accumulation under high-lipid conditions( x ± s, n=3)
A: Effects of ZLY16 at different concentrations on viability of C2C12; B: Representative images of lipid content (red) and eMyHC (green)
expression in C2C12 myoblasts(scale bar: 50 μm); C: Western blotting of PPARβ, CPT-1a and myogenin protein levels in C2C12
myoblasts; D: Quantification of PPARβ protein levels in C2C12 myoblasts; E: Quantification of CPT-1a protein levels in C2C12
myoblasts; F: Quantification of myogenin protein levels in C2C12 myoblasts
# ##
P < 0.05, P < 0.01 vs control group; *P < 0.05, **P < 0.01 vs PA group
能够上调 PPARβ、CPT-1a 和 myogenin 的蛋白表达 C2C12 细胞 PA 来模拟 DMD 患者骨骼肌脂质蓄积
(P<0.05,P<0.01,P<0.05)。以上结果表明,ZLY16 状态,同时给予 PPARβ 激动剂 ZLY16 后考察其脂
能够通过减少 C2C12 细胞中脂质蓄积来促进成肌 质变化及增殖分化情况来进一步探究 ZLY16 是否
细胞分化。 通过改善脂质蓄积从而促进肌再生。结果显示,在
高脂环境下 ZLY16 可以通过减少脂质蓄积从而促
4 讨 论
进成肌细胞分化。因此,后期可以在动物模型上验
本研究发现连续 6 周灌胃 30 mg/kg ZLY16 能 证 PPARβ 激动剂在高脂条件下是否对肌再生有积
够增加 mdx 小鼠肌抓力,降低血清中 TG、TC 含 极作用及进一步探究其具体的分子机制。
量,纠正血脂异常并减少肌肉重量系数,改善骨骼 有研究表明调控 PPARβ 活性可以抑制或促进
肌假性肥大。此外,ZLY16 能够缓解 mdx 小鼠骨 骨骼肌的愈合和再生 [18] 。在骨骼肌再生过程中,
骼肌纤维化,减轻肌纤维坏死和炎性细胞浸润,增 肌卫星细胞发挥主要作用。当骨骼肌损伤时,肌卫
加新生肌纤维数量。综上,ZLY16 通过降低 mdx 星细胞被激活,进入细胞周期,增殖、分化为成肌细
小鼠体内脂质蓄积促进肌再生,从而改善其骨骼肌 胞,最终与受损肌纤维融合或从头生成肌纤维 。
[19]
损伤,恢复运动能力。后期本研究将进一步扩大给 PPARβ 对于卫星细胞的维护以及肌生成非常重要,可
药范围,探究药效与给药剂量之间的关系。 以通过叉头框蛋白 O1(foxhead box protein,FOXO1)
DMD 患者肌肉病理表现为炎性细胞浸润、肌 调节骨骼肌的再生能力 [20−21] 。因此,ZLY16 作为
[1]
纤维坏死、纤维化和大量脂肪占位 。有研究表明, PPARβ 激动剂能够改善 mdx 鼠骨骼肌功能,可能
DMD 患者体内脂质含量异常升高与骨骼肌再生有 是因为能够促进卫星细胞增殖和分化,从而促进新
密切关联 [15−16] 。此外,有研究表明 PPARβ 激动剂 生肌纤维的形成。
GW1516 能够通过上调靶基因 CPT-1a,增强脂肪酸 在 DMD 疾病进程中,慢性炎症持续产生促
氧化,抑制肝脏脂肪生成 [17] 。本研究通过给予 纤 维 化 的 转 化 生 长 因 子 -β1( transforming growth