Page 43 - 《中国药科大学学报》2025年第4期
P. 43
第 56 卷第 4 期 乔振宇,等:调控转录因子 GLI1 与 DNA 相互作用的药物研发策略 439
N
NMe 2 NMe 2 NH OH
High throughput screening SAR
NH HN N CH 3
CH 3
N
H 3 C
Cpd1
Cl Cl K d =207 nmol/L SPR assay
N
OH HN CH 3
O OCH 3
SST0776 Structural modification H
N
Cl N
OH
N JC19
O N
SST0794
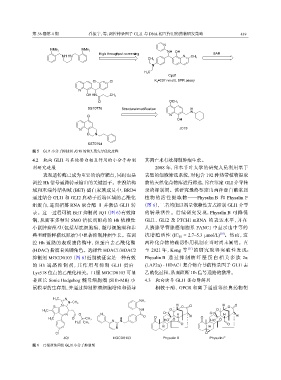
图 5 GLI1 小分子抑制剂 JC19 的苗头到先导优化过程
4.2 靶向 GLI1 与其他蛋白相互作用的小分子抑制 其凋亡来有效抑制肿瘤生长。
剂研究进展 2008 年,日本千叶大学的研究人员利用基于
表观遗传酶已成为重要的治疗靶点,同时也是 表型的细胞筛选系统,对包含 192 种热带植物提取
调控 Hh 信号通路转录输出的关键因子。在溴结构 物的天然化合物库进行筛选,旨在鉴定 GLI 介导转
域和末端外结构域 (BET) 蛋白家族成员中,BRD4 录的抑制剂。该研究最终鉴定出两种源自酸浆属
通过结合 GLI1 和 GLI2 启动子近端区域的乙酰化 植物的活性提取物 ——Physalin B 和 Physalin F
组蛋白,进而招募 RNA 聚合酶 Ⅱ 并激活 GLI1 转 (图 6),二者均能以剂量依赖性方式抑制 GLI1 介导
录。这一过程可被 BET 抑制剂 JQ1 (图 6)有效抑 的转录活性。后续研究发现,Physalin B 可降低
制,从而在多种对 SMO 拮抗剂耐药的 Hh 依赖性 GLI1、GLI2 及 PTCH1 mRNA 的表达水平,并在
小鼠肿瘤模型(包括基底细胞癌、髓母细胞瘤和非 人胰腺导管腺癌细胞系 PANC1 中显示出中等的
[50]
典型畸胎样横纹肌瘤)中显著抑制肿瘤生长。在调 抗增殖活性 (IC = 2.7~5.3 µmol/L) 。然而,这
50
控 Hh 通路的表观遗传酶中,组蛋白去乙酰化酶 两种化合物的确切作用机制在当时尚未阐明。直
(HDAC) 扮演着关键角色。选择性 HDAC1/HDAC2 至 2021 年,Kong 等 [51] 的研究取得突破性发现:
抑制剂 MGCD0103 (图 6)近期被证实是一种有效 Physalin B 通 过 抑 制 核 纤 层 蛋 白 相 关 多 肽 2α
的 Hh 通 路 抑 制 剂 , 其 作 用 与 抑 制 GLI1 蛋 白 (LAP2α) - HDAC1 复合物介导的转录因子 GLI1 去
Lys518 位点的乙酰化相关。口服 MGCD0103 可显 乙酰化过程,从而阻断 Hh 信号通路的激活。
著延长 Sonic Hedgehog 髓母细胞瘤 (SHh-MB) 小 4.3 靶向诱导 GLI1 蛋白降解剂
鼠模型的生存期,并通过抑制肿瘤细胞增殖和诱导 相较于酶、GPCR 和离子通道等经典药物靶
H 3 C N
NH 2
N CH 3
S N H O O H O O
H 3 C NH O O
N O N O H H O H H
H 3 C O CH 3 H O O O O O
N N HO HO
H 3 C CH 3 O O
N H H
Cl O
JQ1 MGCD0103 Physalin B Physalin F
图 6 已报道的间接 GLI1 小分子抑制剂