Page 28 - 《中国药科大学学报》2026年第1期
P. 28
22 学报 Journal of China Pharmaceutical University 2026, 57(1): 19 − 27 第 57 卷
STING 激动剂 STING 激动剂 STING ISAC
瘤内注射给药 静脉全身给药 静脉注射给药
抗体
STING 激动剂
溶酶体
IFN-β, Cxcl10, IFN-γ,
IL-6, TNF-α
Type I IFN
IRF3
STING
STING
激动剂 肿瘤细胞死亡
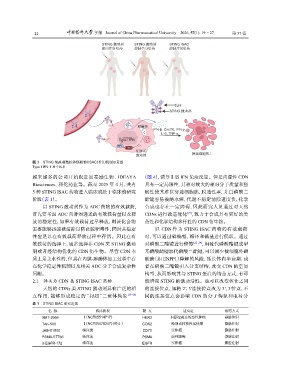
图 3 STING 免疫刺激抗体偶联物(ISAC)作用机制示意图
Type I IFN:Ⅰ型干扰素
越来越多的公司开始跟进如泰励生物、IDEAYA (图 4),诱导Ⅰ型 IFN 免疫反应。但是内源性 CDN
Biosciences、科伦药业等。截至 2025 年 4 月,共有 具有一定局限性,其相对较大的相对分子质量和强
5 种 STING ISAC 药物进入临床或处于临床前研究 极性使其难以穿透细胞膜,膜透性差,并且磷酸二
阶段(表 1)。 酯键容易被酶水解,代谢不稳定清除速度快,化学
以 STING 激动剂作为 ADC 药物的有效载荷, 合成也存在一定障碍,因此研究人员通过对天然
首先要考虑 ADC 向肿瘤递送的有效载荷量以及释 CDNs 进行改造优化 ,致力于合成具有更好的类
[21]
放的稳定性,如果有效载荷过早释放,则该化合物 药性和化学结构多样性的 CDN 衍生物。
需要能够迅速被清除以防止脱靶毒性,同时其稳定 以 CDN 作为 STING ISAC 药物的有效载荷
性应足以在有效载荷释放过程中存活。因此在有 时,可以通过磷酸酯、糖环和碱基进行偶联。通过
效载荷的选择上,通常选择非 CDN 类 STING 激动 对磷酸二酯键进行修饰 [22−24] ,用硫代磷酸酯键或甲
剂或者经结构优化的 CDN 衍生物。尽管 CDN 本 基磷酸酯键取代磷酸二酯键,可以减少被细胞外磷
质上是亲水性的,但其在内膜-溶酶体加工过程中存 酸酶(如 ENPP1)降解的风险,延长体内半衰期,或
在化学稳定性瓶颈以及相关 ADC 分子合成复杂性 者在磷酸二酯键引入分支结构,改变 CDN 的空间
问题。 构型,从而影响其与 STING 蛋白的结合方式,有可
2.1 弹头为 CDN 类 STING ISAC 药物 能增强 STING 的激动活性。也可以改变核苷之间
天然的 CDNs 类 STING 激动剂具有广泛的相 的连接位点,如将 2',3'连接位点改为 3',3'位点,不
互作用,能够形成稳定的“封闭”二聚体构象 [19−20] 同的连接位点会影响 CDN 的分子构象和电荷分
表 1 STING ISAC 研究进展
名 称 临床阶段 靶 点 适应证 给药方式
XMT-2056 Ⅰ(NCT05514717) HER2 HER2表达的恶性肿瘤 静脉注射
TAK-500 Ⅰ(NCT05070247)(终止) CCR2 晚期或转移性实体瘤 静脉注射
JAB-X1800 临床前 CD73 实体瘤 静脉注射
PSMA-E7766 临床前 PSMA 前列腺癌 静脉注射
α-EGFR-172 临床前 EGFR 实体瘤 腹腔注射