Page 62 - 《水产学报》2026年第2期
P. 62
2 期 水 产 学 报 50 卷
+pcDNA3.1-Neh1
−1 109 +26
luc pGL3-NQO1-P5 c
−884 +26
luc pGL3-NQO1-P4 c
−654 +26
luc pGL3-NQO1-P3 a
−488 +26
luc pGL3-NQO1-P2 b
−201 +26
luc pGL3-NQO1-P1 e
pGL3-Basic d
0 4 8 12
相对比值 (荧光/内参)
relative LUC/REN
(a)
ARE1
−654 +26 +pcDNA3.1-Neh1
luc
pGL3-NQO1-P3 a
NQO1-P3-MUT1 (−518/−532)
MT 5'-GAGTACTACATGCTGTCAAAAATG-3' b
MUT1 5'-GAGTAACTTCCCAACACACCAAATG-3' NQO1-P3-MUT2 (−463/−476) d
ARE2
−654 +26 NQO1-P3-MUT1+MUT2 c
luc
pGL3-Basic d
MT 5'-TAGGGGTTGGGGTGCATAAACCTC-3' 0 4 8 12
MUT2 5'-TAGGGACCAAAACATGCGGACCTC-3' 相对比值 (荧光/内参)
relative LUC/REN
(b)
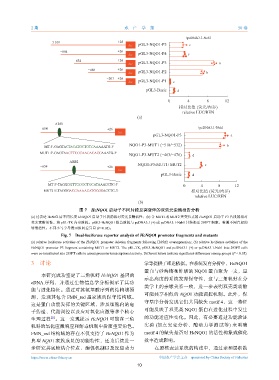
图 7 HcNQO1 启动子不同片段及突变体的双荧光素酶报告分析
(a) 过表达 HcNrf2 后不同长度 HcNQO1 启动子片段的相对荧光素酶活性;(b) 含 MUTI 或 MUT2 突变位点的 HcNQO1 启动子 P3 片段的相对
荧光素酶活性。将 pRL-TK 内参质粒、pGL3-HcNQO1 报告质粒与 pcDNA3.1 (+) 或 pcDNA3.1-Neh1 共转染至 293FT 细胞,检测不同片段的
转录活性。不同小写字母表示组间差异显 (P<0.05)。
Fig. 7 Dual-luciferase reporter analysis of HcNQO1 promoter fragments and mutants
(a) relative luciferase activities of the HcNQO1 promoter deletion fragments following HcNrf2 overexpression.; (b) relative luciferase activities of the
HcNQO1 promoter P3 fragment containing MUT1 or MUT2. The pRL-TK, pGL3-HcNQO1 and pcDNA3.1 (+) or pcDNA3.1-Neh1 into 293FT cells
were co-transfected into 293FT cells to assess promoter transcriptional activity. Different letters indicate significant differences among groups (P < 0.05).
3 讨论 学等提供了理论依据。在系统发育分析中,HcNQO1
蛋白与砂海螂和蚌蛎的 NQO1 蛋白聚为一支,显
本研究成功鉴定了三角帆蚌 HcNQO1 基因的
示出高度的系统发育保守性,这与三角帆蚌在分
cDNA 序列,并通过生物信息学分析揭示了其功
类学上的亲缘关系一致,进一步表明双壳类动物
能与进化特征。通过对其氨基酸序列的结构域预
可能共享相似的 NQO1 功能调控机制。此外,保
测,发现其包含 FMN_red 超家族的保守结构域。
守基序分析发现它们共同缺失 motif 4,这一特征
这是蛋白功能发挥的关键区域,涉及细胞内的电
子传递、代谢调控以及应对氧化应激等多个核心 可能反映了双壳类 NQO1 蛋白在进化过程中发生
生理过程 。这一发现提示 HcNQO1 可能在三角 的功能适应性变化。因此,有必要通过功能验证
[21]
帆蚌的氧化应激响应和解毒机制中扮演重要角色。 实验 (如点突变分析、酶动力学测试等) 来明确
FMN_red 结构域的存在不仅支持了 HcNQO1 作为 motif 4 的缺失是否对 HcNQO1 的活性构象或催化
典型 NQO1 家族成员的功能特性,还为后续进一 效率造成影响。
步研究其底物结合位点、酶促机制以及反应动力 在原核表达系统的构建中,通过亲和层析技
https://www.china-fishery.cn 中国水产学会主办 sponsored by China Society of Fisheries
10