Page 27 - 《爆炸与冲击》2026年第2期
P. 27
第 46 卷 黄 阳,等: 反应平衡对TNT约束爆炸准静态压力热力学模型计算结果的影响 第 2 期
数均与基于吉布斯自由能得出的平衡常数一致。
0
为求解热力学模型,首先假定准静态温度 T 和
d
a
各生成物摩尔数 n 的初值,基于式 (19) 计算对 −10
i
应 T 的各反应平衡常数 K ~K ,然后根据反向
d
8
1
a
传播算法迭代求解温度为 T 时对应的 n ,最后 −20 H 2 ⇌2H
d
a i lgK p O 2 ⇌2O
基于式 (12) 迭代 T ,直至化学反应方程式同时 −30 N 2 ⇌2N
ad
满足反应平衡、质量守恒和能量守恒。在反向 H 2 O⇌H 2 +0.5O 2
H 2 O⇌OH+0.5H 2
传播算法中,基于 K ~K 的表达式可将各生成 −40 H 2 O+0.5N 2 ⇌H 2 +NO
8
1
CO 2 ⇌CO+0.5O 2
物摩尔数 i n C (有固体 CO⇌C+0.5O 2
n 均表示为
、
、
−50
、
n H 2
n N 2
n O 2
n CO (无固体碳析出时)的函数,将 1 000 2 000 3 000 4 000
碳析出时)或
T/K
n 代入到质量守恒方程后,质量守恒方程的残差
i
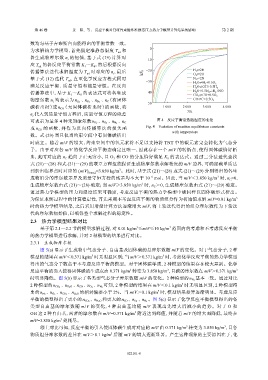
可表示为最多 4 种未知摩尔数 n H 2 、 n O 2 、 n N 2 、 n C 图 4 反应平衡常数随温度的变化
或 n CO 的 函 数 , 并 作 为 反 向 传 播 算 法 的 损 失 函 Fig. 4 Variation of reaction equilibrium constants
with temperature
数。式 (29) 当且仅当约束空间中有固体碳析出
时成立。随着 m/V 的增大,约束空间中的氧元素将不足以支持将 TNT 中的碳元素完全转化为气态分
子。由于对应各 m/V 的化学反应平衡态确定且唯一,因此存在一个 m/V 的转折点,使得固体碳恰好析
出,此时对应的 n 趋向于正无穷小,且 O 和 2 CO 的分压恰好满足 K 的表达式。通过二分法迭代查找
C
8
式 (21)~(28) 和式 (21)~(29) 的联立方程组能保证生成物摩尔数求解精度的 m/V 边界,可确定碳单质达
到析出临界点时对应的 (m/V) trans,2 =3.850 kg/m 。此时,基于式 (21)~(28) 或式 (21)~(29) 分别得出的各生
3
成物组分的摩尔数差异及质量守恒方程的残差均不大于 10 mol。因此,当 m/V<3.850 kg/m 时,n =0,
−6
3
C
生成物摩尔数由式 (21)~(28) 确定;当 m/V≥3.850 kg/m 时,n >0,生成物摩尔数由式 (21)~(29) 确定。
3
C
通过热力学模型的压力和温度结果可确定,考虑反应平衡的热力学模型中碳同样以固体碳形式析出。
为保证求解过程中的计算稳定性,首先采用不考虑反应平衡的物质组分作为初始值求解 m/V=0.01 kg/m 3
时的热力学模型结果,之后采用增量计算方法逐渐增大 m/V,将上轮迭代得出的组分摩尔数作为下轮迭
代的摩尔数初始值,以确保整个求解过程的稳定性。
2.3 热力学模型结果对比
3
3
基于第 2.1~2.2 节的模型求解过程,对 0.01 kg/m ≤m/V≤10 kg/m 范围内的考虑和不考虑反应平衡
的热力学模型进行求解,并对 2 种模型的结果进行对比。
2.3.1 生成物摩尔数
图 5(a) 显示了生成物中气态分子、自由基及固体碳的总摩尔数随 m/V 的变化。对于气态分子,2 种
3
模型的结果在 m/V<0.371 kg/m 时无明显区别;当 m/V>0.371 kg/m 时,考虑化学反应平衡的热力学模型
3
得出的气态分子数高于不考虑反应平衡的模型。对于固体碳单质,2 种模型的结果存在较大差别。化学
3
3
反应平衡的引入使得固体碳的生成点由 0.371 kg/m 转变为 3.850 kg/m ,且碳的摩尔数在 m/V>0.371 kg/m 3
时明显降低。图 5(b) 显示了各类型气态分子摩尔数随 m/V 的变化。2 种模型的 n N 2 基本一致。通过对比
3
2 种模型的 n CO 2 、 n H 2 O 、 n CO 、 n O 2 、 n N 2 可知,2 种模型的结果在 m/V<0.1 kg/m 时无明显区别,2 种模型得
3
n H 2 O 的相对偏差小于 2%。当 m/V>0.1 kg/m 时,模型结果差异逐渐明显。考虑反应
出的 n N 2 、 n O 2 、 n CO 2 、
。图 5(c) 显示了化学反应平衡模型得出的各
平衡的模型得出了更小的 n CO 2 、 n H 2 O 和更大的 n CO 、 n O 2 、 n H 2
类 型 自 由 基 的 摩 尔 数 随 m/V 的 变 化 , 4 种 自 由 基 均 随 m/V 表 现 出 先 增 大 后 减 小 的 趋 势 。 对 于 O 和
3
OH 这 2 种自由基,两者的摩尔数在 m/V=0.371 kg/m 附近达到峰值,并随着 m/V 的增大而降低,最终在
3
m/V=3.850 kg/m 处耗尽。
综上对比可知,反应平衡的引入使固体碳生成时对应的 m/V 由 0.371 kg/m 转变为 3.850 kg/m ,且各
3
3
物质组分摩尔数的差异在 m/V>0.1 kg/m 后随 m/V 的增大逐渐显著。产生这种现象的主要原因在于,化
3
022101-8