Page 12 - 《中国药科大学学报》2026年第2期
P. 12
138 学报 Journal of China Pharmaceutical University 2026, 57(2): 133 − 143 第 57 卷
O H O O OH O O
HO N OH HO OH HO OH HO OH
O OH O O O
NOG, 1 2 3 4
O O O O O O O
HO OH HO OH HO OH HO OH
O OH OH N
5 6 7 8
Cl O
OH H O H
N
N N I HO N OH HO N OH
OH OH N O O
9 10 11 12 13
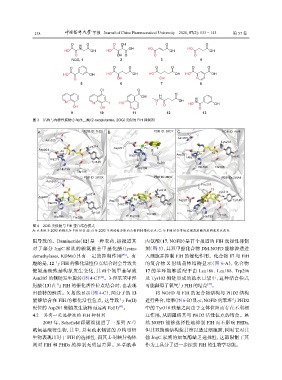
图 3 结构与内源性底物 2-氧戊二酸(2-oxoglutarate, 2OG)类似的 FIH 抑制剂
A PDB ID: 1H2K B PDB ID: 3KCY C PDB ID: 4AI8
Asn205
Asn205 Lys214
Lys214
Asp201 Zn Asp201 Fe 9
1 His279 Asp201 Zn 12 Tyr145
His279 His279
Tyr145 Ile281
His199 His199 His199 Thr196
Thr196
PDB ID: 2W0X PDB ID: 4BIO PDB ID: 2WA4
Asn205
Phe207
Lys214 13
11 Lys214
Lys214
Asp201
Fe Asp201 Fe Asp201 Tyr145
His279 His279 Ile281 Tyr145 Fe 13
8
His279
Tyr145 Thr196
His199 Thr196 His199 His199 Thr196
图 4 2OG 类似物与 FIH 蛋白结合模式
A:以类似于 2OG 的模式与 FIH 结合;B:以与 2OG 不同的螯合取向占据 FIH 催化位点;C:与 FIH 结合导致关键氨基酸残基构象发生改变
阻导致的。Daminozide(12)是一种农药,据报道其 丙氨酸(17,NOFD)是首个报道的 FIH 选择性抑制
对于部分 JmjC 家族的赖氨酸去甲基化酶(lysine 剂(图 5),其双甲酯化合物 DM-NOFD 能够渗透进
demethylases,KDMs)具有一定的抑制作用 。有 入细胞并抑制 FIH 的催化作用。化合物 17 与 FIH
[45]
趣的是,12 与 FIH 的催化活性位点结合时会导致关 的复合物 X 射线晶体结构显示(图 6-A),化合物
键氨基酸残基构象发生变化,其两个氮甲基导致 17 的苯环能够适配于由 Leu186、Leu188、Trp296
Asn205 的侧链发生旋转(图 4-C) 。3-羟基苯甲羟 及 Tyr102 侧链形成的疏水口袋中,这种结合模式
[46]
肟酸(13)在与 FIH 的催化活性位点结合时,也表现 可能阻碍了氧气与 FIH 的结合 。
[47]
出独特的性质。X 射线显示(图 4-C),两分子的 13 将 NOFD 与 FIH 的复合物结构与 PHD2 结构
能够结合在 FIH 的催化活性位点,这导致与 Fe(II) 进行叠合,结果(图 6-B)显示,NOFD 的苯环与 PHD2
配位的 Asp201 侧链发生旋转而远离 Fe(II) 。 中的 Tyr310 残基之间由于立体位阻而存在不利相
[43]
4.2 具有一定选择性的 FIH 抑制剂 互作用,从而阻碍其与 PHD2 活性位点的结合。虽
2005 年,Schofield 课题组报道了一系列 N-草 然 NOFD 能够选择性地抑制 FIH 而不影响 PHDs,
酰氨基酸衍生物,其中,具有疏水侧链的 D 构型衍 但其双羧酸结构使其难以透过细胞膜,同时它对其
生物表现出对于 FIH 的选择性,而其 L-对映异构体 他 JmjC 家族的加氧酶缺乏选择性,这都限制了其
则对 FIH 和 PHDs 的抑制无明显差异。N-草酰苯 作为工具分子进一步探索 FIH 的生物学功能。