Page 136 - 《中国药科大学学报》2026年第1期
P. 136
130 学报 Journal of China Pharmaceutical University 2026, 57(1): 122 − 132 第 57 卷
A
OH OH OH NH
NH O
N O O H OH
N
O H O O O A L A G A H
H 2 N N N N OH N N OH HN N N H O N
O N O O H O N O N
H
H
Californibin Pseudosporamide Micitide
OH OH
N
B
N N N
H O H O
O N O
MRYYH BytO N OH MNYLH BytO HN NH
MRYFH N O H O NH OH
H
O
R
YYH R=OH Myxarylin
YFH R=H
OH O NH
N N O
MRYLH P450 blt H O MRYLW P450 blt O OH
O N HN HN
N HN O
N O H OH O
H O
P450 blt 产物(MRYLH) P450 blt 产物(MRYLW)
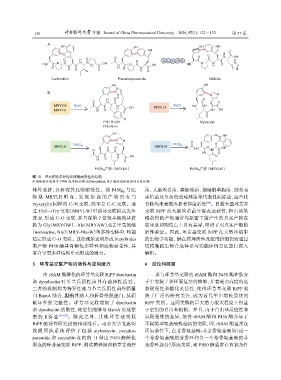
图 10 具有催化多样性和底物耐受性的结构
A:前体肽具有保守 YPW 基序的结构;B:Biarylitides 类产物的前体肽序列以及结构
体外表征,以研究其底物耐受性。将 P450 与底 菌、大肠埃希菌、粪肠球菌、铜绿假单胞菌、肺炎克
t
bl
物 肽 MRYLH 孵 育 , 发 现 形 成 的 产 物 具 有 与 雷伯菌及金黄色葡萄球菌等代表性病原菌,这些化
myxarylin 同样的 C–N 交联,而不是 C–C 交联。通 合物均未表现出显著抑菌活性 。目前大量环芳基
[44]
过 His5→Trp 突变(MRYLW)可诱导交联模式发生 交联 RiPP 由大肠埃希菌异源表达获得,但由该策
改变,形成 C–O 交联,并且在第 2 位氨基酸残基替 略获得的产物通常与原宿主菌产生的真实产物在
换为 Gly(MRYGW)、Ala(MRYAW)或去甲亮氨酸 前导肽切割位点上具有差异,阻碍了对真实产物的
(norleucine,Nle)(MRY-Nle-W)等多种变体中,均能 活性验证。因此,环芳基交联 RiPP 在天然环境中
稳定形成 C–O 交联。这些现象表明形成 biarylitides 的生物学功能、潜在药理活性及应用价值仍需通过
类产物 P450 酶具有催化多样性和底物耐受性,具 更精准的生物合成体系与功能评价方法进行深入
有介导更多样结构单元形成的潜力。 解析。
5 环芳基交联产物的活性与应用潜力 6 结论和展望
由 rSAM 酶催化的环芳基交联 RiPP darobactin 参与环芳基交联的 rSAM 酶和 P450 酶在肽分
和 dynobactin 对革兰氏阴性菌具有选择性活性。 子中安装了多样而复杂的修饰,并表现出高度的底
二者的机制均为特异性地与革兰氏阴性菌外膜蛋 物耐受性和催化灵活性,使得环芳基交联 RiPP 收
白 BamA 结合,阻断其插入和折叠外膜蛋白,从而 获了广泛的研究关注,成为近几年中增长最快的
破坏外膜完整性。环芳基交联增加了 darobactin RiPP 类别。这两类酶的巨大潜力很大程度上得益
和 dynobactin 的刚性,使它们能够与 BamA 形成紧 于它们的自由基机制。并且,由于自由基反应性和
密 的 β 折 叠 [51−52] 。 除 此 之 外 , 其 他 环 芳 基 交 联 氧耐受性的差异,使得 rSAM 酶和 P450 酶介导了
RiPP 的活性研究进展相对滞后。南京大学戈惠明 不同类型氨基酸残基间的交联,即,rSAM 酶通常在
教 授 团 队 系 统 评 估 了 包 括 arylomycin、 pseudos- 厌氧条件下,在芳香氨基酸-非芳香氨基酸间(或一
poramide 和 spectabin 在内的 11 种由 P450 酶催化 个芳香氨基酸的芳香环和另一个芳香氨基酸的非
形成的环芳基交联 RiPP,测试菌株涵盖枯草芽孢杆 芳香环部分)形成交联,而 P450 酶通常在有氧条件