Page 33 - 《渔业研究》2026年第2期
P. 33
176 渔 业 研 究 第 48 卷
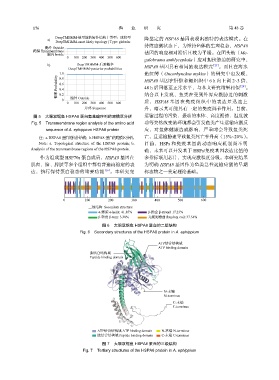
DeepTMHMM-最可能的拓扑结构丨类型:球状型 隆鉴定的 基因表现出独特的表达模式。在
a) HSPA8
DeepTMHMM-most likely topology | Type: globular
持续应激状态下,为维持鱼体的生理稳态,HSPA8
胞外 Outside
跨膜 Transmembrane
胞内 Inside 基因的响应相对滞后且较为平缓。在团头鲂(Me-
0 100 200 300 400 500 600
galobrama amblycephala)应对拥挤胁迫的研究中,
b) DeepTMHMM-后验概率 基因具有相同的表达模式 [23] 。而且在海水
DeepTMHMM-posterior probabilities HSPA8
1.0 鱼虹鳟(Oncorhynchus mykiss)的研究中也发现,
概率 Probability 0.6 HSPA8 后回落至正常水平,与本文研究结果相似 [24] 。
0.8
内上调
基因在肝脏和鳃组织中
2~3 倍,
6 h
48 h
0.4
0.2
0 胞外 Outside 结合以上发现,鱼类在受到外界应激胁迫的刺激
基因在免疫组织中的表达量迅速上
0 100 200 300 400 500 600 后,HSPA8
序列 Sequence 升,暗示其可能具有一定的免疫调节作用。目前,
图 5 大眼双锯鱼 HSPA8 蛋白氨基酸序列的跨膜区分析 运输过程的污染、振动的水体、高度拥挤、温度波
Fig. 5 Transmembrane region analysis of the amino acid 动等突然改变的环境都会引发鱼类产生运输应激反
sequence of A. ephippium HSPA8 protein 应,对鱼体健康造成影响,严重时会导致鱼类死
注:a. HSPA8 蛋白的拓扑结构;b. HSPA8 蛋白的跨膜区分析。 亡,且运输胁迫导致鱼类死亡率升高(15%~20%) 。
Note: a. Topological structure of the HSPA8 protein; b. 目前,HSPs 和免疫基因的动态响应机制尚不明
Analysis of the transmembrane regions of the HSPA8 protein. 确,未来可以开发基于 HSPs/免疫基因表达比值的
作为组成型 HSP70s 蛋白成员,HSPA8 基因在 多指标联用芯片,实现应激程度分级。本研究结果
肌肉、脑、脾脏等多个组织中都有普遍而稳定的表 为明确 HSPA8 基因作为鱼类急性运输应激的早期
达,执行保持蛋白稳态的重要功能 [16] 。本研究克 标志物之一奠定理论基础。
0 100 200 300 400 500 600
二级结构 Secondary structure:
α-螺旋 α-helix: 41.85% β-折叠 β-strand: 17.23%
β-转角 β-turn: 3.38% 无规则卷曲 Random coil: 37.54%
图 6 大眼双锯鱼 HSPA8 蛋白的二级结构
Fig. 6 Secondary structures of the HSPA8 protein in A. ephippium
ATP结合结构域
ATP binding domain
肽结合结构域
Peptide binding domain
N-末端
N-terminus
C-末端
C-terminus
ATP结合结构域 ATP binding domain N-末端 N-terminus
肽结合结构域 Peptide binding domain C-末端 C-terminus
图 7 大眼双锯鱼 HSPA8 蛋白的三级结构
Fig. 7 Tertiary structures of the HSPA8 protein in A. ephippium